一.化学式
1.定义:用元素符号和数字的组合表示物质组成的式子
2.写法和读法:
(1)单质的化学式

双原子:H2、N2、O2、Cl2(氯气)等
多原子:O3(臭氧)、P4(白磷)等
(2)化合物的化学式
① 氧化物的写法和读法:
写法:氧元素写在后面,另一种元素写在前面,并标出角码,当角码为“1”时省略 。
读法:角码为1时,读作“氧化某” ,如:ZnO(氧化锌)、MgO(氧化镁)等。
角码不为1时,读作“几氧化几某” ,如:Fe3O4(四氧化三铁)、P2O5(五氧化二磷)等。
特殊:H2O(水)、CO(一氧化碳)、Fe2O3(氧化铁)、FeO(氧化亚铁)、H2O2(过氧化氢)等
②由一种金属元素和一种非金属元素组成的化合物的写法和读法:
写法:金属元素在前,非金属元素在后,并标出角码,当角码为“1”时省略 。
读法:读作“某化某”,如:NaCl(氯化钠)、MgCl2(氯化镁)、ZnS(硫化锌)等
特殊:FeCl2(氯化亚铁)、FeCl3(氯化铁)
3.化学式表示的含义:
以H2O为例:
(1)从组成上看:
宏观:水是由氢元素和氧元素组成的;
微观:水是由许多水分子构成的,一个水分子是由两个氢原子和一个氧原子构成的。
(2)从它代表的物质看:
宏观:水这种物质;
微观:一个水分子。
说明:只要化学式前有化学计量数(旧称“系数”),只表示微观。
如:3H2O 表示三个水分子、2Fe 表示两个铁原子等。
二.相对分子质量(M r)
1.定义:化学式中所有原子相对原子质量之和
说明:是一个比值,单位为“1”
2.有关化学式的相关计算:
(1)相对分子质量、相对分子质量总和的计算:
例如:水(H2O)的相对分子质量为:2×1+1×16 = 18 或 Mr(H2O) = 2×1+1×16 = 18
CuSO4· 5H2O的相对分子质量为:64+32+16×4 + 5×(2×1+16) = 250
(说明:化学式中的“·”此时表示“+”,而不是数学中的“×”)
2CO2的相对分子质量总和为:2×(12+16×2) = 88
(2)化合物中原子个数比或元素质量比的计算:
例如:求NH4NO3中各原子个数比、各元素的质量比
NH4NO3中氮原子、氢原子、氧原子的个数比为2∶4∶3;
NH4NO3中氮元素、氢元素、氧元素的质量比为(2×14)∶(4×1)∶(3×16)= 7∶1∶12
或者NH4NO3中m(N)∶m(H)∶m(O) = (2×14)∶(4×1)∶(3×16)= 7∶1∶12
(3)化合物中元素质量分数的计算
例如:求NH4NO3中氮元素的质量分数
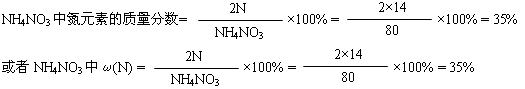
三.化合价
1.定义:一种元素的一定数目的原子与其它元素一定数目的原子化合时所表现出的性质。
说明:化合价是元素的一种性质。
2.分类及写法:
(1)分类:正价:+1、 +2、+3、+4、+5、+6、+7 负价:-1、-2、-3、-4
(2)写法:写在元素符号的正上方,正负号在前,数字在后。(注意:“1” 不能省略)
例如:

3.化合物中元素化合价的规律及特点:
(1)在化合物中,氢元素一般显+1价,氧元素一般显 –2 价;
金属元素只显正价,K、Na、Ag 一般只显+1价,Ca、Mg、Ba、Zn一般只显+2价。
(2)常见的变价元素:①非金属元素,如:Cl在化合物中可显-1、+1、+3、+5、+7价
②金属元素,如:Fe在化合物中可显+2、+3价
(3)原子团的化合价在数值上等于其所带的电荷数
| 常见原子团 | 符号 | 化合价 |
| 氢氧根离子 | OH- | -1 |
| 硝酸根离子 | NO3- | -1 |
| 硫酸根离子 | SO42- | -2 |
| 碳酸根离子 | CO32- | -2 |
| 铵根离子 | NH4+ | +1 |
(4)一种元素在一种化合物中可以显示不同价态,如:NH4NO3中氮元素的化合价
(5)规定:单质中,元素化合价为零。(可以从化合价的定义理解)
(6)法则:化合物中,元素正负化合价的代数和为零。
(7)初中阶段常见化合价的口诀:
一价氯氢钾钠银,二价氧镁钙钡锌,
三铝四硅五价磷,二三铁二四碳,
二四六硫三五氮,铜汞二价最常见。
4.化合价的应用:
(1)求未知元素的化合价
例如:求高锰酸钾(KMnO4)中锰元素的化合价
设锰元素的化合价为x,同时标出常见元素的化合价,如K为+1价,O为-2价,根据化合物中元素化合价
代数和为零的原则,可以列式:(+1)×1+ x·1 + (-2)×4 = 0 ,则x = +7
(2)根据化合价,书写化学式:
即正前,负后,约简交叉。

(同学们也可以根据书上的方法进行书写)
(3)根据化合价,判断化学式的正误
【例题解析】
A.N2 、NH3、NO2 B.NH3、N2O5、NO2
C.N2、N2O3、NH3 D.NH3、N2、N2O3
【分析】 A中N元素的化合价依次为0,-3价,+4价;B中N元素的化合价依次为-3价,+5价,+4价;C中N元素的化合价依次为0,+5价,-3价;D中N元素的化合价依次为-3价,0,+5价。
【正确答案】D
(1)离子个数的是__________;(2)离子所带电荷数值的是__________。
(3)分子个数的是__________;(4)元素化合价数值的是__________。
【分析】化学式前面的数字表示粒子个数,如2CO表示两个一氧化碳分子,2Ag+表示两个银离子;化学式中元素符号右下角的数字表示一个分子中含有这种原子的个数,如H2O中的“2”表示一个水分子中含有两个氢原子;元素的化合价与离子电荷的表示方法有严格的区别,化合价标在元素符号正上方,且符号在前,数字在后,例
【正确答案】(1)② (2)③ (3)① (4)④
请回答下列问题:
(1)传统食品加工过程中,一般在1kg面粉中含有1g明矾(已知:明矾的化学式为KAl(SO4)2·12H2O,其相对分子质量是474;1g = 1000mg)。试求:
① 1g明矾中含铝元素__________ mg;
② 该200g食品中含铝元素__________ mg;
③ 体重为50kg的某同学一天食用该食品150g,他摄入的铝量__________(选填“已”或“未”)超过安全摄入量。
(2)为降低铝的摄入量,请你提出两条建议。
①__________;② __________。
【分析】
明矾的化学式为KAl(SO4)2·12H2O,这一化学式含有结晶水,比较复杂。
Mr[KAl(SO4)2·12H2O]=39+27+(32+4×16)×2+12×(2×1+16)=474,其中“· ”计算时为“+”,要计算铝元素的质量,先计算出铝元素的质量分数,然后根据某元素的质量=化合物的质量×该元素的质量分数。
ω(Al)=(27÷474)×100%=5.7%,m(Al)=1g×5.7%=0.057g=57.0mg;因为1kg面粉中含有1g明矾,即面粉中含明矾的质量分数为0.1%,所以200g食品中含有明矾的质量约为0.2g,其中铝元素的质量=0.2g×5.7%=11.4mg;
某同学摄入的铝元素质量为150g×0.1%×5.7%=8.55 mg < 0.7 mg×50=35 mg,未超过安全摄入量。
【正确答案】57.0mg 11.4mg 未
①生活中减少铝制品的使用,②少喝易拉罐饮料,③减少服用含铝的药品。
A.1-3a % B.1-2a % C.1-a % D.3a %
【分析】FeSO4和Fe2(SO4)3两化合物由铁、硫、氧三元素组成,按常规解法要求铁元素质量分数,必须知道硫和氧质量分数,而题目只给出了硫元素质量分数,似乎无法求解,但若认真分析其组成特点,不难看出在混合物中,有一个硫原子必定对应四个氧原子,因此硫元素与氧元素的质量比是固定的。
根据上述分析可知:硫元素与氧元素的质量比为
【正确答案】A
