1.下列物质排放到空气中,不会使空气受到污染的是( )
A.煤和石油等燃料燃烧后产生的废气
B.化工厂产生的烟尘
C.机动车辆排放的尾气
D.绿色植物光合作用产生的气体
2.氩气是一种稀有气体,若以●表示氩原子,则氩气是以下列何种形式存在?
A.
 B.
B. C.
C. D.
D.
3.不需其他试剂就能区别的一组溶液是( )
A.FeCl3 NaOH KCl Ba(NO3)2
B.NaCl Na2CO3 KNO3 HCl
C.Na2SO4 BaCl2 K2CO3 KNO3
D.BaCl2 CuSO4 NaOH NaCl
4.小明等四名同学以“寻找常温下能加速过氧化氢分解的物质.并通过实验比较它们的效果”为课题开展研究,他们的研究报告中有下列说法,你认为正确的是( )
A.氧化铜是由氢氧化铜和稀硫酸反应制得
B.氧化铁是由铁在氧气中燃烧制得
C.通过多次对比实验都发现氧化铜的加速效果好于铜丝,因而得出初步结论:氧化铜对过氧化氧分解的加速作用好于铜丝
D.从氧化铁的加速效果好于铁丝,就可认定氧化物的加速作用好于单质
5.如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分
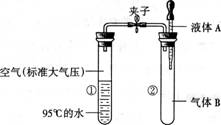 反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合可能是下列的( )
反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合可能是下列的( )A.水、一氧化碳
B.硫酸、氮气
C.酒精、氧气
D.氢氧化钠溶液、二氧化碳
6.某同学检测刚从小商店买回的食盐是否是加碘食盐[加碘食盐中的碘元素以碘酸钾(KIO3)形式存在]。经过查阅资料得知碘酸钾(KIO3)在酸性条件下能与KI溶液发生反应生成碘(I2),I2遇淀粉变蓝色。现提供下列试剂和生活中常见的物质:①米汤、②纯碱、③KI溶液、④白糖、⑤白酒、⑥白醋。该同学进行检验必须用到的试剂和物质是( )
A.①③④ B.①③⑥ C.②④⑥ D.①④⑤
7.往AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完成后再过滤,不可能存在的情况是( )
A.滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+
B.滤纸上有Ag 、Cu,滤液中有Zn2+、Fe2+
C.滤纸上有Ag 、Cu、Fe, 滤液中有Zn2+、Fe2+
D.滤纸上有Ag 、Cu、Fe 、Zn,滤液中有Zn2+、Fe2+
8.小分子团水是航天员专用水,具有饮用少、在人体内储留时间长、排放量少等特点。一次饮用125 mL小分子团水,可维持人体6 h正常需水量。下列关于小分子团水的说法中,正确的是( )
A.水分子的化学性质被改变了
B.小分子团水中水分子间没有间隔
C.小分子团水中的水分子停止了运动
D.小分子团水的部分物理性质与普通水有所不同
9.植物进行光合作用时,需不断消耗空气中的二氧化碳,但二氧化碳在大气中的含量却基本保持不变,这是由于( )
①动植物的呼吸作用 ②矿物燃料的燃烧
③死亡动植物的腐烂 ④某些矿物如CaCO3等的加热分解
A.①③ B.①④ C.①② D.①②③④
10. 某种即热饭盒用混有少量铁粉的镁粉与水反应提供热量。现将该混合物分成四等份,进行如下实验,其中实验操作和现象与实验结论相符的是( )
| 实验操作和现象 | 实验结论 | |
| A. | 用磁铁充分接触该混合物,磁铁上吸附有少量黑色粉末 | 用化学方法可以分离镁和铁 |
| B. | 将该混合物加入到一定量的稀硫酸中,有气泡产生,反应结束后有固体剩余 | 剩余固体中一定有铁 |
| C. | 向该混合物中加入少量水,剧烈反应放出大量热,有气泡产生 | 该气体一定是氧气 |
| D. | 将该混合物加入到一定量的硫酸铜溶液中,反应结束后有固体剩余 | 剩余固体中一定有铜,一定没有镁 |
11.能证明澄清透明的矿泉水是混合物的实验是( )
A.将矿泉水通电,看其能否分解
B.加入肥皂水后振荡,看能否出现丰富的泡沫
C.向水中通入二氧化碳,看其能否出沉淀
D.滴在洁净的玻璃片上,观察蒸发后是否留有痕迹
12.某同学为了探究使带火星的木条复燃的氧气是否一定为纯氧气,若否,则使带火星木条复燃的氧气含量极限是多少?为此该同学按下表所示比例,用排水法收集氧气进行实验:
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | |
| 空气体积分数/% | 50 | 70 | 75 | 80 | 85 |
| 排水体积分数/% | 50 | 30 | 25 | 20 | 15 |
| 带火星木条复燃情况 | 复燃 | 复燃 | 复燃 | 火星明亮, 时燃时不燃 |
火星稍变明亮, 不复燃 |
(1)该实验说明使带火星的木条复燃的氧气______(选填“一定”或“不一定”)是纯氧气。
(2)氧气的体积分数大于_____________________时,就能使带火星的木条复燃。
(3)从该实验可知:氧气的物理性质为:____________;化学性质为:____________。
13.喷泉是一种常见的自然现象,其产生的原因是存在压强差。在化学实验中经常也可以形成美丽的喷泉。
(1)在甲图的装置中,倒置于铁架台的圆底烧瓶中充满干燥的O2气体,连接在瓶塞上的导管伸入到装有水的烧杯中(此时止水夹关闭)。不久即可看到白磷自己燃烧起来。待白烟消失,烧瓶冷却后,打开止水夹,可以观察到烧瓶内形成美丽的喷泉。产生该现象的原因用化学方程式表示___________________。
(2)某同学积极思考后,设计了如图乙的装置,也
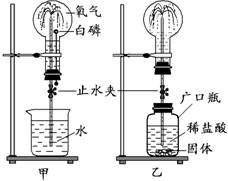 同样形成了喷泉。已知该同学在广口瓶中装入的是稀盐酸和另一种固体物质,待它们反应完全后,打开止水夹,在上方的烧瓶内也形成喷泉。该同学加入的固体物质不可能是
同样形成了喷泉。已知该同学在广口瓶中装入的是稀盐酸和另一种固体物质,待它们反应完全后,打开止水夹,在上方的烧瓶内也形成喷泉。该同学加入的固体物质不可能是 A、锌粒(Zn)
B、碳酸钙(CaCO3 )
C、木炭(C)
D、镁(Mg)
(3)比较甲、乙两套装置,从产生喷泉的原理来分析,甲装置是_______(填“增大”或“减小”)上部烧瓶内气体压强;乙装置是_______(填“增大”或“减小”)下部广口瓶内气体压强。
(4)城市中常见的人造喷泉以及自然界的火山爆发原理与上述________(填“甲”或“乙”)装置的原理相似。
14. 某无色气体可能含有N2、H2、CO、CO2中的一种或几种,将该气体依次通过下列各种药品(假设每一步反应均完全)。

试根据流程图回答问题:
(1)该气体中(填“一定”、“可能”或“肯定不”)__________含有氢气。
(2)写出上述实验中一定能发生反应的化学方程式______________________________
___________________________________________________________________。
(3)根据现象和数据推断原气体的所有可能组成:
____________________________________________________________________
【参考答案】
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| 答案 | D | A | D | C | D | B | D | D | D | B | D |
13.4P + 5O2
14.(1)一定
(2)H2+CuO
(3) ①H2 CO2 ②H2 CO2 N2 ③H2 CO2 CO ④H2 CO2 CO N2
