1.“雪碧”是一种无色的碳酸饮料,将少量“雪碧”滴入紫色石蕊试液中,然后再加热,溶液的颜色变化情况是:
A.先变红后变紫 B.变红后颜色不再改变
C.先变无色后变红 D.先变蓝后变紫
2.下列关于二氧化碳的用途只利用了其物理性质的是
A.二氧化碳用作灭火剂
B.干冰能用于人工降雨
C.二氧化碳能用来生产汽水等碳酸饮料
D.二氧化碳参加绿色植物的光合作用可提高农作物产量
3.有关CO2的实验中,能达到实验目的是
A.将燃着的木条放在集气瓶口,检验CO2是否收集满
B.用向下排气法收集一瓶CO2气体,观察CO2的颜色
C.将CO2气体通入紫色石蕊试液中,证明CO2溶于水显酸性
D.将CO2气体通入CaCl2溶液中,可以看到有白色沉淀生成
4.实验室制取CO2时,向盛有石灰石的锥形瓶中加入酸后,过一会儿石灰石表面几乎无气泡产生,其原因可能是( )
A. 没有加热
B. 锥形瓶上的橡皮塞漏气
C. 加入的酸是硫酸
D. 没有用玻璃捧搅拌反应物
5.检验一种气体是否是CO2的可靠方法是( )
A. 通入澄清的石灰水,看石灰水是否变浑浊
B. 将燃着的木条伸入气体中看火焰是否熄灭
C. 检验该气体的密度是否比空气密度大
D. 通入水中看溶解性
6.将二氧化碳通入澄清石灰水中,有白色沉淀生成,若继续通入二氧化碳,白色沉淀完全溶解。其反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O、CaCO3+CO2+H2O=Ca(HCO3)2(易溶)。当二氧化碳持续不断的通入澄清石灰水中时,沉淀质量的变化符合图中的
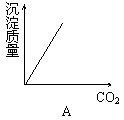
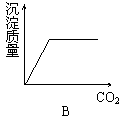
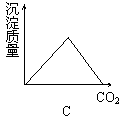

7.某气体M中可能含有H2、CO、CO2和水蒸气中的一种或几种。把M通入灼热的盛有足量氧化铜的试管,充分反应后,管内物质质量减少0.8 g。将反应后的气体通过盛有足量浓硫酸的洗气瓶,洗气瓶中物质增重0.8 g。气体M的组成不可能是
A.H2、CO、水蒸汽 B.H2、CO2、CO
C.H2、CO2、水蒸汽 D.H2、CO2、CO、水蒸汽
8.实验室现有高锰酸钾、稀硫酸、稀盐酸、石灰石、棉花及以下仪器:
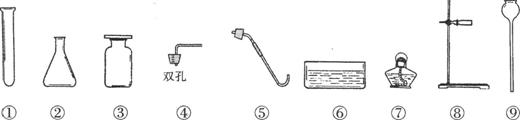
(1)利用上述药品实验室制取氧气所需
 要的仪器是__________(填序号);
要的仪器是__________(填序号);制取该气体的化学方程式为_______________________
(2)请写出实验室制取二氧化碳的化学方程式:_______________
将制取二氧化碳的发生装置图画入方框内,并与A装置连接:
实验过程中A装置内的实验现象是_____________________。
由此得出的结论是_____________________________________。
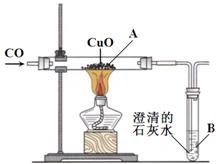 9.右图为一氧化碳还原氧化铜的装置图:
9.右图为一氧化碳还原氧化铜的装置图:(1)图中A、B两处的实验现象是:
A处____________________________________,
B处___________________________________。
(2)一氧化碳还原氧化铜的化学方程式是____________,该反应说明一氧化碳具有________性。
(3)该装置中存在的主要问题是____________________,改进的具体方法是______________________。
10.下列为小萍同学在实验室制取CO2并检验CO2性质的实验装置示意图。试回答:
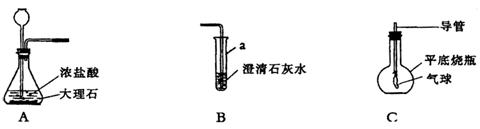
(1)仪器的名称;a__________;
(2)用化学方程式表示实验室制取CO2的反应原理__________________________________。
(3)该同学在实验过程中,将A中产生的气体通入到B中,观察到澄清石灰水没有变浑浊,试分析其原因_________________________________________________________。
(4)该同学用C瓶收集满一瓶由装置A中产生的气体后,往瓶中倒入浓氢氧化钠溶液,迅速用事先绑好一个小气球的胶塞塞紧,振荡,可以观察到小气球逐渐膨大。其原因是_________________________,请写出C中反应的化学方程式____________________________。
11.化学兴趣小组的同学们在实验室发现一些黑色粉末,是做“碳还原氧化铜”的实验时剩余的药品,于是对其成分进行探究。
【猜想与实验设计】小红猜测:黑色粉末是CuO。她设计了如下图所示的实验装置。

【实验步骤】取适量该粉末放入玻璃管中,打开K通入CO,排尽空气后加热。
| 现 象 | |
| A装置 | 黑色粉末逐渐变成红色 |
| B装置 | 澄清石灰水变浑浊 |
【实验结论】该黑色粉末是CuO。B装置中反应的化学方程式为_____________________。
【评价与反思】
(1)小芸认为该实验装置存在安全隐患,需要改进的是_________________________;
小芸还认为小红的实验结论是有欠缺的,她认为该黑色粉末的成分是_________________,
理由是______________________________________________。
(2)小红经过反思,改进了实验并确认了黑色粉末的成分。请填写下表。
| 实验步骤 | 实验现象 | 实验结论 |
|
|
参考答案:
1.A 2.B 3.AC 4.C 5.A 6.C 7.C
8.
(1)①③⑤⑥⑦⑧;
 2KMnO4
2KMnO4 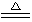 K2MnO4 + MnO2 + O2 ↑
K2MnO4 + MnO2 + O2 ↑(2) CaCO3 + 2HCl = CaCl2 + H2O + CO2 ↑;
二氧化碳的发生装置如右图:
燃着的蜡烛由下至上依次熄灭;
二氧化碳的密度大于空气的密度,且不支持燃烧。
9.
(1)黑色粉末变成光亮的红色 澄清石灰水变浑浊
(2)CuO+CO
 Cu+CO2 还原性
Cu+CO2 还原性(3)尾气没有处理 增加集气装置或放置酒精灯点燃,将尾气燃烧转化为无毒的二氧化碳气体
10.
(1)试管
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)浓盐酸挥发出的氯化氢气体随二氧化碳进入澄清石灰水中
(4)二氧化碳被氢氧化钠吸收,导致平底烧瓶内的压强减小,导致空气被压入小气球中,所以小气球逐渐膨大。
2NaOH+CO2=Na2CO3+H2O
11.
【实验结论】Ca(OH)2+CO2 = CaCO3↓+H2O
(1)增加尾气处理装置 一定含氧化铜,也可能是混有炭粉的氧化铜 含有炭粉的氧化铜也能出现同样的实验现象
(2)
| 实验步骤 | 实验现象 | 实验结论 |
| ①关闭K,②取适量该粉末放入玻璃管中,③加热。 | 若A中黑色粉末变红,B中的澄清石灰水变浑浊。 | 该黑色粉末是炭粉和氧化铜的混合物。 |
| 若A、B中均无明显现象。 | 该黑色粉末是氧化铜。 |
