1.地壳中含量最多的非金属元素是( )
A.氧元素 B.铁元素 C.硅元素 D.铝元素
2.一瓶气体经过检验得出其中只有一种元素,则该气体不可能是( )
A.一种单质 B.一种混合物 C.纯净物 D.一种化合物
3.下列说法错误的是( )
A.分子是化学变化中的最小微粒
B.氧气和臭氧(O3)都是由同种元素组成的
C.H和O质子数不同
D.在化学变化中分子可以再分
4.日常生活常接触到“含氟牙膏”、“高钙牛奶、碘盐”、“富硒茶叶”、“加铁酱油”等用品,这里的氟、钙、碘、硒、铁指的是( )
A.单质 B.原子 C.元素 D.离子
5.元素周期表是学习化学的重要工具,下图是元素周期表中的一格,下面从该
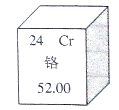 图获取的信息中,正确的是( )
图获取的信息中,正确的是( )A.该元素的原子序数为52
B.该元素属于非金属元素
C.该元素在地壳中的含量为52.00%
D.该元素的原子核外有24个电子
6.为纪念俄国化学家门捷列夫,101号元素被命名为钔,其元素符号的正确写法是( )
A.mD B.Md C.MD D.md
7.下列关于微观粒子的说法,正确的是
A.原子是由分子构成的。
B.原子中含有质子、中子和核外电子。
C.原子若失去核外电子,则会变成阴离子。
D.原子若得到核外电子,则会变成阳离子。
8.镁原子与镁离子在结构上具有相同的 ( )
A.核电荷数 B.最外层电子数 C.电子层数 D.电子数
9.化合物MCl2种,M元素原子核内的质子数可能为( )
A.1 B.10 C.11 D.12
10.朝核问题引发了国际关注,核问题的关键是核能的如何利用。已知某种核原料的原子核中含有1个质子和2个中子,那么
A.该原子是一种氢原子 B.该元素是金属元素
C.该原子核外有3个电子 D.该原子核带2个单位的正电荷
11.下列各组微粒中,属于同一种元素的是
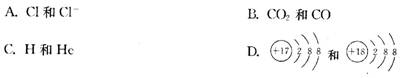
12.化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和,如用“613C”表示核内有6个质子和7个中子的碳原子。下列对1735Cl和1737Cl的判断中,正确的是( )
A.原子中含有相同数目的中子
B.原子中核外电子数不同
C.属于同种元素
D.原子核内质子数目不同
13.下列各组数字代表了元素的核电荷数,其中能组成A2B型离子化合物的一组是( )
A. 11和8 B.12和17 C.8和12 D.11和18
14.M元素的离子为M2-,其核外电子数为a,核内中子数为b,则M的相对原子质量为( )
A. a+b+2 B.a+b-2 C.a+b D.b+2
15.从下列粒子的结构示意图得出的结论中,错误的是 ( )
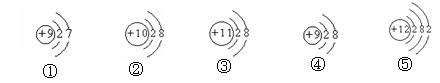
A.①④属于同种元素 B.②③④属于离子
C.⑤易失去电子成为阳离子 D.①⑤的结构不稳定
二、填空题
1.图A是元素周期表的一部分
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第二 周期 |
3 Li 锂 7 |
4 Be 铍 9 |
5 B 硼 11 |
① | 7 N 氮 14 |
8 O 氧 16 |
9 F 氟 19 |
10 Ne 氖 20 |
| 第三 周期 |
11 Na 钠 23 |
② | 13 Al 铝 27 |
14 Si 硅 28 |
③ | 16 S 硫 32 |
17 Cl 氯 35.5 |
18 Ar 氩 40 |
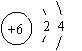 图C
图C 
(1)原子序数为14的元素名称为_________;
(2)图B是某元素的原子结构示意图,该元素在图A中的位置是(填①或②或③)_________;
(3)图C是氯元素的原子结构示意图,图A中与氯元素在同一纵行的氟元素,其原子结构与氯原子相似。由此推测,氟原子在化学反应中易(填“得”或“失”)_________电子。
2.有A,B,C,D 4种微粒,A微粒带一个单位正电荷,原子核外无电子;B为原子,其元素在地壳里含量最多;C微粒带有2个单位负电荷,其核外有3个电子层;D原子的核外有3个电子层,最外层有3个电子。试写出A,B,C,D 4种微粒的符号:A为_____;B为_____;C为_____;D为_____。
3.下图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
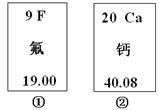
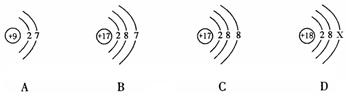
请你回答:
(1)氟元素的相对原子质量为__________,钙元素的原子序数为__________;
(2)X=__________;
(3)A、B、C、D属于同种元素的粒子是__________(填序号);
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似__________(填序号)
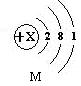 4.M元素的单质可用于原子反应堆的导热剂,其原子结构示意图如右:
4.M元素的单质可用于原子反应堆的导热剂,其原子结构示意图如右:(1) 该原子有_____个电子层,X的值是__________,
M元素属于__________(填“金属”或“非金属”)元素;
(2) M元素的化学性质与下列__________(填序号)元素的化学性质相似。

(3) M元素的离子符号是__________;(用元素符号填空,下同)
(4) M元素和第(2)小题的D元素形成化合物的化学式是__________。
5.下图表示的是地壳里所含各种元素的质量分数。请根据右图回答:
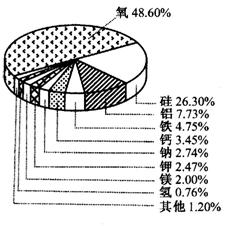
(1)图中表示出的金属元素有_____种;
(2)地壳中所含铝元素的质量分数为__________;
(3)氢元素与地壳中含量最多的非金属元素之间,形成的化合物是__________。
6.元素周期表是学习和研究化学的重要工具。下图是元素周期表的一部分。
| IA | O | |||||||
| 1 | 1 H 1.008 |
ⅡA | ⅢA | ⅣA | V A | ⅥA | ⅦA | 2He 4.003 |
| 2 | 3 Li 6.941 |
4 Be 9.012 |
5 B 10.8l |
6 C 12.01 |
7 N 14.0l |
8 0 16.00 |
9 F 19.00 |
10 He 20.8l |
| 3 | 11Na 22.99 |
12Mg 24.31 |
13 Al 26.98 |
14 Si 28.09 |
15 P 30.97 |
16 S 32.06 |
17 Cl 35.45 |
18Ar 39.95 |
(2)查出碳的相对原子质量:__________,写出16号元素的元素符号:__________。
(3)表中不同种元素最本质的区别是__________(填符号)。
A.质子数不同, B.中子数不同 C.相对原子质量不同 D.电子数不同
(4)利用元素周期表,人们对元素的认识进入全新的飞跃时期。近年,俄罗斯科学家曾宣布他们将人工合成第1 18号元素,则此元素的核电荷数为__________。
(5)周期表中每一个横行叫做一个周期,第三周期开头元素和靠近尾部元素的原子结构示意图分别为

根据以上信息,可以得到的结论是________________________________________。
参考答案
一.选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | A | D | A | C | D | B | B | A | D | A |
| 题号 | 11 | 12 | 13 | 14 | 15 | |||||
| 答案 | A | C | A | B | B | |||||
二.填空题
1.硅 ① 得
2.A:H+;B:O;C:S2-;D:Al
3.(1)19.00;20 (2)8 (3) B C (4) B
4.(1)3 11 金属; (2)A (3) Na+ (4) Na2S
5.6 7.73% 水、过氧化氢
6.
(1)门捷列夫或道尔顿或张青莲等
(2)12.01 S
(3)A
(4)118
(5)第三周期开头元素的原子易失电子成为阳离子或第三周期靠近尾部元素的原子易得电子成为阴离子或活泼金属与活泼非金属易通过得失电子发生化学反应
