碳的化合物种类繁多,尤其是有机化合物在国民经济的发展中起着非常重要的作用。而碳的氧化(CO和CO2)不仅与日常生活密切相关,同时也是初中化学元素化合物知识中非常重要的一部分,碳和碳的氧化物是以后学习许多化学反应的基础,初中化学的许多反应都与碳和碳的氧化物有关。
一、二氧化碳
1.二氧化碳的物理性质
在通常情况下,
 二氧化碳是无色无味气体,相同条件下密度比空气大,能溶于水,1体积的水约能溶解1体积的二氧化碳,增大压强还会溶解得更多。生产汽水等碳酸型饮料就是利用了二氧化碳的这一性质。
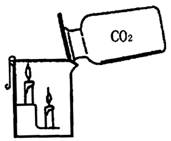
二氧化碳是无色无味气体,相同条件下密度比空气大,能溶于水,1体积的水约能溶解1体积的二氧化碳,增大压强还会溶解得更多。生产汽水等碳酸型饮料就是利用了二氧化碳的这一性质。很多实验在证明二氧化碳的物理性质的同时也能体现出二氧化碳的化学性质。右图倾倒CO2的实验,根据现象“烧杯底下的蜡烛先熄灭”,可以验证“在相同条件下,CO2的密度比空气大,不能燃烧,也不支持燃烧”的这一性质。
CO2的溶解性实验:如右图所示,在收集满CO2的空塑料矿
 泉水瓶里加入适量的蒸馏水,振荡,塑料瓶子变瘪,可以证明CO2能溶于水。再加入紫色石蕊溶液,溶液变红,加热后又变成紫色,证明CO2溶于水的同时能与水反应:
泉水瓶里加入适量的蒸馏水,振荡,塑料瓶子变瘪,可以证明CO2能溶于水。再加入紫色石蕊溶液,溶液变红,加热后又变成紫色,证明CO2溶于水的同时能与水反应:H2O+CO2=H2CO3;H2CO3=H2O+CO2↑
根据教材实验的设计:(Ⅰ)向干燥的紫色石蕊小花(纸花)喷稀醋酸;(Ⅱ)向干燥的紫色石蕊小花喷水;(Ⅲ)直接把干燥的紫色石蕊小花放入干燥的二氧化碳中;(Ⅳ)将干燥的紫色石蕊小花喷水后放入二氧化碳中;(Ⅴ)将(Ⅳ)中小花取出后小心加热。通过观察实验现象,可以得出以下结论:
(1)石蕊是一种酸碱指示剂,遇酸变成红色。
(2)水不能使紫色石蕊变成红色,干燥的二氧化碳也不能使紫色石蕊变成红色。
(3)二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊变成红色。
(4)碳酸不稳定,容易分解成二氧化碳和水。
2.二氧化碳的化学性质
(1)一般情况下,二氧化碳不能燃烧,也不支持燃烧,不供给呼吸。
(2)二氧化碳跟水反应生成碳酸,碳酸能使紫色石蕊溶液变红色。
CO2+H2O=H2CO3(紫变红)
碳酸不稳定,很容易分解成水和二氧化碳,所以红色石蕊又变成紫色,
H2CO3=H2O+CO2↑(红变紫)
(3)二氧化碳跟石灰水反应:CO2+Ca(OH)2=CaCO3↓+H2O(清变浊)
3.二氧化碳的用途:
二氧化碳不支持燃烧,不能燃烧,且比空气重,将二氧化碳覆盖在燃着的物体表面,可使物体跟空气隔绝而停止燃烧,因此二氧化碳可用于灭火,是常用的灭火剂。
在食品工业上,生产碳酸饮料、啤酒、汽水等都需要二氧化碳。
固态的二氧化碳即“干冰”,主要用作致冷剂,或用飞机在高空喷撒“干冰”,可以使空气中水蒸气冷凝,形成人工降雨。
用于贮藏粮食、水果、蔬菜。用二氧化碳贮藏的食品由于缺氧和二氧化碳本身的抑制作用,可有效地防止食品中细菌、霉菌、虫子生长,避免变质和有害健康的过氧化物产生,并能保鲜和维持食品原有的风味和营养成分。二氧化碳不会造成谷物中药物残留和大气污染。用二氧化碳通入大米仓库24 h,能使99%的虫子死亡。
二氧化碳用于工业制纯碱和尿素,促进植物的光合作用,用作气体肥料等。
4.温室效应
大气中的二氧化碳气体能像温室的玻璃或塑料薄膜那样,使地面吸收的太阳光的热量不易散失,从而使全球变暖,这种现象叫温室效应。
温室效应的危害性后果是:
①冰川融化和海平面上升。事实上,冰川融化已经开始,发展下去,海面将升高,一些沿海城市将被海水淹没;
②频繁、严重的旱灾;
③更多更厉害的沙尘暴;
④更频繁更厉害的飓风;
⑤更频繁更严重的森林火灾;
⑥野生动物濒临灭绝。
能产生温室效应的气体不只是二氧化碳,还有甲烷、氟里昂等气体。
二、二氧化碳的制取
1.实验室制取二氧化碳的反应原理
实验室常用大理石或石灰石与稀盐酸反应制取:
CaCO3+2HCl=CaCl2+H2O+CO2↑
注意:
(1)石灰石跟稀硫酸反应,开始有气体产生,过一会儿气泡逐渐减少,以至反应停止。
(2)碳酸钠跟稀盐酸反应十分剧烈,迅速产生大量气体。石灰石跟稀盐酸反应比碳酸钠缓和,也能生成大量气体。
(3)用硫酸代替盐酸跟石灰石反应,虽能产生二氧化碳,但是生成的硫酸钙微溶于水。它会覆盖在块状石灰石表面,阻止碳酸钙跟硫酸接触。而碳酸钠跟盐酸反应太快,生成的二氧化碳不容易收集。因此,实验室里通常是用石灰石跟稀盐酸反应来制取二氧化碳的。
2.实验室制取二氧化碳的装置
(1)实验室制取气体的装置是根据所需药品的状态,反应条件来确定的。制
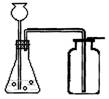 取二氧化碳的反应物石灰石(或大理石)是块状固体,盐酸是液体,反应是在常温下进行的,不需要加热。反应前可以将固体置于锥形瓶中,液体在制取时从长颈漏斗中注入,液体与固体接触时生成的气体经导气管导入集气瓶中。
取二氧化碳的反应物石灰石(或大理石)是块状固体,盐酸是液体,反应是在常温下进行的,不需要加热。反应前可以将固体置于锥形瓶中,液体在制取时从长颈漏斗中注入,液体与固体接触时生成的气体经导气管导入集气瓶中。(2)气体的收集方法主要取决于气体的密度及其在水中的溶解性。由于二氧化碳的密度大于空气又能溶于水,故不宜用排水法收集,所以一般用向上排空气集气法收集二氧化碳。
(3)因为普通漏斗颈太短,产生的二氧化碳气体会从漏斗处逸出。长颈漏斗下端管口必须液封,也就是说为了避免产生的气体从漏斗中逸出,必须使长颈漏斗的下端管口在液面以下。
(4)锥形瓶在装置中作为容器,可以用其他(如大试管、烧瓶、广口瓶)口径大小适宜的容器代替。
(5)根据二氧化碳不能燃烧、不支持燃烧的性质,可以将燃着的木条放在集气瓶口,如火焰熄灭,则二氧化碳已收集满。
3.实验室制取氧气、二氧化碳比较
| 氧气 | 二氧化碳 | |
| 反应原理 | 2KMnO4 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑2H2O2 |
CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| 发生装置 | 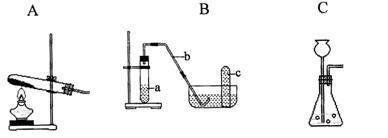 | |
| 用高锰酸钾在加热制氧气可用装置A 用过氧化氢和二氧化锰制取可用装置B 石灰石和稀盐酸制CO2可用装置C | ||
| 收集方法 | 向上排空气法、排水法 | 向上排空气法 |
| 检验方法 | 用带火星木条伸入集气瓶中,若木条复燃该气体是氧气 | 将气体通入澄清石灰水,若石灰水变浑浊说明该气体是CO2 |
三、一氧化碳
1.一氧化碳的物理性质
在通常状况下,一氧化碳的是无色、无味气体,难溶于水。在相同条件下,一氧化碳的密度略小于空气。
根据一氧化碳的物理性质,在实验室应用排水集气法收集。不能用向下排空气法收集。因为一氧化碳无色,无法知道气体是否集满,而且一氧化碳有毒,长时间收集会使实验者中毒。
2.一氧化碳的化学性质
(1)可燃性
一氧化碳能燃烧,发出蓝色火焰,放出大量的热,生成一种能使澄清石灰水变浑浊的无色气体。
2CO+O2
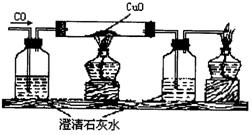
(2)一氧化碳的还原性
一氧化碳不仅有可燃性,还具有还原性。
原因是它们都夺取含氧化合物中的氧,使其还原:
CO+CuO
 CO2+Cu
CO2+Cu可以用右图完成实验:
3.一氧化碳的毒性和对空气的污染
一氧化碳有剧毒!一氧化碳被人吸进肺中,极易跟血液中的血红蛋白结合。一氧化碳跟血红蛋白的结合能力比氧气大200倍~300倍,造成机体急性缺氧。当一氧化碳在空气中浓度为0.02%时,人在2 ~3 小时后就会出现头晕恶心的症状;浓度达0.08%时,2小时即昏迷;浓度再高,将危及生命。
4.一氧化碳的用途
一氧化碳可作气体燃料和用来冶炼金属,工业上利用一氧化碳的还原性,在炼铁厂把铁矿石还原成铁:
Fe2O3+3CO
【例题解析】
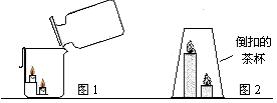
(1)小聪和小明受到老师的启发,设计了如图2的家庭小实验,并推测了实验现象。
两位同学都认为蜡烛会熄灭,因为__________________________________________。
但对图2中“两支蜡烛谁先熄灭?”的问题却有不同的看法:
小明认为低的蜡烛先熄灭,理由是____________________________;
小聪认为高的蜡烛先熄灭,理由是____________________________。
(2)通过实验,证明小聪的看法是正确的,同时还观察到茶杯内壁变黑。
你认为茶杯变黑的可能原因是_________________________________________。
(3)由上述实验得到启发:从意外失火的高楼中逃生的正确方法是_________(填序号)。
①用毛巾捂住口鼻 ②低头弯腰沿墙迅速移向门外 ③打开窗户跳出
【分析】在相同条件下,二氧化碳的密度大于空气,因此将二氧化碳沿着烧杯壁倒入时就像将水倒入烧杯一样,二氧化碳流到烧杯底部,又由于二氧化碳本身不燃烧且不支持燃烧将燃着的蜡烛和氧气隔绝,导致下面的蜡烛熄灭。随后二氧化碳继续上涨使上面的蜡烛也熄灭了。
(1)蜡烛燃烧消耗氧气,同时产生二氧化碳,由于二氧化碳不可燃,也不支持燃烧,因此可以推断蜡烛会熄灭。一般同学们都会认为二氧化碳的密度在相同条件下比空气大,因此从图1将实验结论迁移过来判断下面的蜡烛先熄灭。但是同学们忽略了图2实验中的二氧化碳不是实验者倒入的,而是蜡烛燃烧产生的热的二氧化碳,温度较高的二氧化碳密度会变小,进而集中在蜡烛上方隔绝空气使蜡烛熄灭。
(2)蜡烛是由碳元素和氢元素组成的,茶杯内壁的黑色物质是蜡烛在氧气不充足的情况下产生的。
(3)因为着火时燃烧生成的二氧化碳因为温度高密度小集中上面,因此低头弯腰迅速逃生可以减少晕倒的可能性。用毛巾捂住口鼻可以减少烟尘,如果是湿毛巾效果更好。没有经过专业训练的人采取跳窗的方式逃生的死亡几率会比较高,不应采用。
本题答案:
密度比空气密度大、不能燃烧、不能支持燃烧
(1)杯内的氧气被耗尽同时又产生了不能燃烧且不能支持燃烧的气体
蜡烛燃烧产生的CO2密度大会下沉
蜡烛燃烧使高处的氧气量逐渐减少并耗尽,同时放出的热使CO2向上扩散浓度增大
(2)蜡烛在氧气不充足的条件下燃烧生成了炭黑
(3)①②
A. CO2 B. O2 C. H2 D. CO
【分析】CO与血红蛋白的结合能力要比氧气与血红蛋白结合能力大200~300倍,一旦一氧化碳与血红蛋白结合,就会阻止氧气与血红蛋白的正常结合,造成肌体急性缺氧,因此一氧化碳有剧毒。为了大家的身体健康应该劝自己的亲友少抽烟,最好不抽烟。
本题答案:D
(1)下列实验操作中不正确的是________(填标号)。
①制备气体前检查装置的气密性 ②加热实验结束时,用嘴吹灭酒精灯
③将用剩的药品放回原试剂瓶中
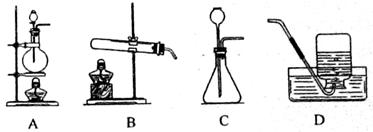
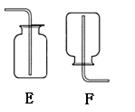
(2)在实验室里,可用浓盐酸与二氧化锰在加热条件下起反应制取氯气(Cl2),该气
 体能溶于水,则制取氯气应选择的发生装置和收集装置分别是________(填标号)。
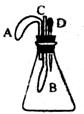
体能溶于水,则制取氯气应选择的发生装置和收集装置分别是________(填标号)。(3)某兴趣小组设计的趣味小实验装置如右图所示,其中A、B为未膨胀的气球,C为玻璃导管,D为胶头滴管。用气密性良好的该装置分别进行甲、乙两组实验。实验时均把胶头滴管中的溶液(足量)加入到锥形瓶中,并轻轻振荡。请填写下表中的空白:(CO2+ 2NaOH = Na2CO3 + H2O)
| 锥形瓶中的物质 | 胶头滴管中的物质 | 观察到气球(A、B)的变化 | 有关反应的化学方程式 | |
| 甲 | 二氧化碳 | 浓氢氧化钠溶液 | ||
| 乙 | A气球胀大 B气球无明显变化 |
(4)取12g石灰石(主要成分是CaCO3,杂质不参加反应)放入烧杯中,向其中加入100g一定质量分数的稀盐酸,二者恰好完全反应。反应结束后,称量烧杯中剩余物质的总质量为107.6g(不包括烧杯的质量,且气体溶解忽略不计)。则参加反应的碳酸钙的质量是多少?稀盐酸中溶质的质量分数是多少?
【分析】
(1)为保证气体顺利的收集到气体,在气体制备前认真检查装置的气密性是非常有必要的。吹灭酒精灯会导致酒精灯爆炸,是一个非常危险的操作。取用药品时用剩下的药品放回原瓶很可能造成对原瓶试剂的污染,正确的操作应该是放到老师指定的容器内。
第(2)小题是对选择制气体装置原则的进一步考查,根据反应物的状态,一固一液只能从AC中选择,因为B中盛放液体浓盐酸会顺着导管完全留出试管,并且该反应需要加热,即需要酒精灯,所以只能从AC中选择A装置。因为氯气能溶于水因此不能用排水法收集,而氯气的密度比空气大因此可以用向上排空气法收集。
第(3)小题甲组实验二氧化碳和浓氢氧化钠会发生反应CO2+ 2NaOH = Na2CO3 + H2O,生成的物质中没有气体,因此瓶内气体减少,导致瓶内压强小于大气压,进而是瓶内气球膨胀。如果要让A气球变大,需要让瓶内产生气体使瓶内气压大于大气压,因此选择一个能产生气体的反应即可。
第(4)小题计算时要注意代入化学方程式计算的数据必须参加反应或反应生成的纯净物的质量,而题目中所给数据都是混合物的质量,因此需要另辟蹊径,根据质量守恒定律,计算反应前后烧杯中物质的质量之差为产生气体的质量。气体质量计算出后,就变成一道简单的化学方程式计算了。
本题答案:
(1)②③
(2)A、E
(3)
| 锥形瓶的物质 | 胶头滴管中的物质 | 观察到气球(A、B)的变化 | 有关反应的化学方程式 | |
| 甲 | B气球胀大 A气球无明显变化 |
CO2+ 2NaOH = Na2CO3 + H2O | ||
| 乙 | 二氧化锰或碳酸钠等 | 双氧水或盐酸等 | 2H2O2MnO22H2O+O2↑ (或Na2CO3 +2HCl== 2NaCl+H2O+CO2↑等) |
解:生成二氧化碳的质量为:12g+100g – 107.6g = 4.4g
设参加反应的碳酸钙的质量为x,稀盐酸中氯化氢的质量为 y。
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
100 73 44
x y 4.4g
答:参加反应的碳酸钙为10g;稀盐酸中溶质的质量分数为7.3%。
