(一)固体溶解度
1.概念:在一定温度下,某固态物质在100 g溶剂(通常溶剂为水)里达到饱和状态时所溶解的质量。
溶解度的概念包括四个要素:
①指明一定温度;②溶剂为100 g;③必须达到饱和状态;④单位为g。
影响固体溶解度的外界因素:温度
2.“易溶”、“可溶”、“微溶”、“难溶”等表示的意思:
| 溶解度/g | >10 | 1~10 | 0.01~1 | <0.01 |
| 溶解性 | 易溶 | 可溶 | 微溶 | 难溶 |
3.溶解度曲线
用纵坐标表示溶解度,横坐标表示温度,绘制出的溶解度随温度而变化的曲线叫做溶解度曲线。通过溶解度曲线,可以判断固体物质的溶解度受温度影响的变化情况,可以
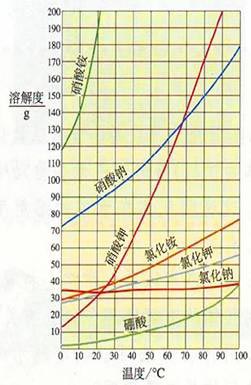 比较不同物质在同一温度时溶解度的大小,也可以查出同一种物质在不同温度时的溶解度。
比较不同物质在同一温度时溶解度的大小,也可以查出同一种物质在不同温度时的溶解度。三种典型的固体溶解度曲线:
(1)溶解度受温度影响较大,如:KNO3
(一般采用冷却热饱和溶液的方法获得晶体)
(2)溶解度受温度影响较小,如:NaCl
(一般采用蒸发溶剂的方法获得晶体)
(3)溶解度随温度的升高而减小,如Ca(OH)2
溶解度曲线表示的有关信息:
①某物质在某温度时的溶解度;
②可以比较同一物质在不同温度时的溶解度;
③可以比较不同物质在同一温度时的溶解度;
④曲线的交点所表示某一温度下不同物质的溶解度相同的。
⑤物质的溶解度受温度影响的变化情况;
(二)气体的溶解度
1.概念:气体的溶解度是指在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。
影响气体溶解度的因素:温度和压强。一般情况下,气体的溶解度随外界压强的增大而增大;随温度的升高而降低。
气体溶解度在实际测定时比较复杂,非标准状况下的数据还应该换算成标准状况下的值。
固体溶解度和气体溶解度的比较:
| 固体溶解度 | 气体溶解度 | |
| 外界条件 | 在一定温度下 | 在压强为101kPa和一定温度时 |
| 衡量标准 | 溶剂(通常指水)量为100g | 1体积水里 |
| 溶液状态 | 饱和 | 饱和 |
| 单位 | 溶解溶质的质量(克g) | 溶解气体的体积(无单位) |
| 影响其大小的外界因素 | 温度 | 温度和压强 |
二、溶质的质量分数(第1课时)
溶液的浓稀、有色溶液的颜色都可以粗略的表示一定量的溶液中含有溶质的多少,溶液中溶质的质量
分数可以准确地表示一定量的溶液中含有溶质的多少。
1.定义:溶液中溶质的质量分数是溶质质量与溶液质量之比。
数学表达式:
特点:无单位、是个比值、一般不受温度的影响等。
饱和溶液溶质的质量分数的计算:
2.配制溶质质量分数一定的溶液
以配制100g溶质质量分数为5%的氯化钠溶液为例分析:
(1)计算:计算配制100g溶质质量分数为5%的氯化钠溶液所需氯化钠和水的质量。
(2)称量:用托盘天平称量所需的氯化钠。
(3)量取:用量筒量取所需的水(水的密度近似看作1g/cm3)。
(4)溶解:将量好的水倒入盛有称量好氯化钠的烧杯中,用玻璃棒搅拌,使氯化钠溶解。
(5)装瓶、贴签:把配制好的溶液装入试剂瓶中,盖好瓶塞并贴上标签,备用。
操作示意图可简单表示如下:

说明:如果用液体溶质来配制溶质质量分数一定的溶液,其步骤为:计算→量取→溶解→装瓶、贴签。想一想,这是为什么?
【例题解析】
A.100g水溶解36g食盐恰好能配成饱和溶液
B.200C时,100g食盐饱和溶液里含有36g食盐
C.200C时,把136g食盐饱和溶液蒸干,可得到36g食盐
D.饱和食盐水溶液中溶质、溶剂、溶液的质量比为36:100:136
解析:本题重在考查大家对于溶解度概念的理解。溶解度这一概念有如下四个要点:一定的温度;100g溶剂;达到饱和状态;质量单位(g)。根据溶解度的概念并结合题给条件可知,A的说法是不正确的,原因在于没有指明温度这一条件;按照溶解度的含义,在20℃时将36g食盐溶于100g水中恰好达到饱和状态,这时所得到的食盐饱和溶液的质量为136g;相反,如果将这136g的食盐饱和溶液蒸干,一定就能得到36g食盐;同样,由于在136g食盐饱和溶液里含有36g食盐,那么,在100g食盐饱和溶液里就不可能含有36g食盐了(肯定比36g要少)。至于饱和食盐水溶液中溶质、溶剂、溶液的质量之比,如果没有温度这一前提条件,就无法进行相应的求算。
答案:C。
A.用量筒量取水时仰视读数
B.配制溶液的烧杯不干燥,留有少量的水
C.氯化钠晶体不纯
D.转移已配好的溶液时,有少量溶液溅出
解析:配制一定溶质质量分数的溶液是一个定量实验,所用试剂不当或操作错误都会给实验结果带来一定的影响。影响的结果如何,我们是可以通过溶质质量分数的计算公式来作出判断的。对于A,这样量取的水的体积要比理论上的体积大一些,其质量也相应变大,因此配得的溶液中氯化钠的质量分数将偏小;对于B,此时相当于所用水的质量增大了,会引起溶液中氯化钠的质量分数偏小;C,当氯化钠晶体不纯时,相当于溶质的质量减小,这样就会引起溶液中氯化钠的质量分数偏小;D在将溶液配制完成之后,即便有少量溶液溅出,但不会影响其中氯化钠的质量分数。
答案:D。
方法一:用5700g清水漂洗,"拧干"后残留在衣服上的洗涤剂质量为(用分数表示,下同)______g;
方法二:用5700g清水均匀分成质量相等的三份(每份1900g),分三次漂洗:
第1次,用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂质量为______g;
第2次,用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂质量为______g;
第3次,用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂质量为______g。
由以上计算分析,用相同质量的水漂洗衣服,是一次漂洗效果好,还是将水分成三份,分三次漂洗效果好?
解析:这是一道密切联系生活实际的简单计算题。试题旨在通过简单计算,使大家明白并掌握节约用水的一种方法。通过这种方法的介绍,引导我们进一步树立节约水、爱惜水的观念,做到合理地利用水、科学地节约和保护水。其实,该题的实质是关于溶质溶解、溶液稀释的计算。它以日常生活中的小事为背景,将漂洗衣服时为什么要“少量多次”的科学道理让学生通过计算加以感受,既考查了分析与计算能力,又进行了节约用水的方法教育,真可谓“匠心独具”,是一道难得的好题。
解答时要注意:题中“拧干后湿衣服上残留的溶液仍为 100g ”,这就意味着不论用什么方法、进行哪一次漂洗,这“ 100g溶液 ”始终应跟随在计算的过程中。如用方法2进行第一次漂洗,漂洗时所用“水”的总质量就应当是: 1900g+100g=2000g,“拧干”后残留在衣服上的洗涤剂质量的质量分数为: 100g×1%÷2000g=0.05% ,因此,残留在衣服上的洗涤剂的质量为:0.05%×100g=1/20 g。
方法一:用5700g清水一次漂洗,拧干后残留再衣服上的洗涤剂的质量为
1g×100g/(100g+5700g)=1/58g
方法二:将5700g水分三次漂洗(每次1900g)
第一次,用1900g清水漂洗,拧干后残留在衣服上的洗涤剂的质量为
1g×100g/(100g+1900g)=1/20g
第二次,再用1900g的水漂洗,拧干后残留在衣服上的洗涤剂的质量为
1/20g×100g/(100g+1900g)=1/400g
第三次,用1900g的清水漂洗。拧干残留再衣服上的洗涤剂的质量为
1/400g×100g/(100g+1900g)=1/8000g
答案:1 1/58 1/20 1/400 1/8000
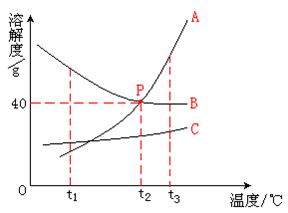
(1)P点表示的含义是___________________
(2)t3℃时,A、B、C三者的溶解度大小关系为____________
(3)将t1℃时B的饱和溶液升温至t3℃,此时溶液的质量______ (填“增大、减小、不变”)
(4)t2℃时,将20g B溶解到60g水中,得到的溶液为_________(填“饱和溶液、不饱和溶液”)
(5)从C的饱和溶液中获得C晶体的最佳方法为___________
(A、蒸发溶剂法 B、冷却热饱和溶液 )
(6)如何从A与B的饱和溶液中获得B物质?_________
【分析】此题综合考查了溶解度曲线的应用以及结晶、有关溶解度的基本计算等知识。
(1)P点表示在t2℃时,A、B两种物质的溶解度相同为40g
(2)很显然,从图像上可以看出,t3℃时,SA>SB>SC
(3)由于B物质的溶解度随温度的升高而减小,所以t1℃时B的饱和溶液升温至t3℃时将会有溶质B析出,所以溶液的质量将会减少。
(4)因为在t2℃B物质的溶解度为40g,即在100g水中最多能溶解40g B物质,那么20g B物质溶解到50g水中便达到饱和,所以t2℃时,将20g B溶解到60g水中,得到的溶液为不饱和溶液。
(5)因为C物质的溶解度随温度的变化较小,所以从C的饱和溶液中获得C晶体的最佳方法为蒸发溶剂法,选(A)
(6)因为A物质随温度的升高而增大,而B物质随温度的升高而降低,所以可以采用升温的方法来获得B物质。
