《北京市化学中考说明》中的要求
| 考试内容 | 考试要求 | 目标层次 | |
| 仪器的使用和基本操作 | 常见的仪器 | 能识别试管、烧杯、烧瓶、锥形瓶、酒精灯、集气瓶、漏斗、长颈漏斗、玻璃棒、量筒、水槽、蒸发皿、胶头滴管(滴瓶)、药匙、燃烧匙、试管夹、铁架台(含铁夹、铁圈)和托盘天平等仪器。 | ★★ |
| 基本操作 | 1.会取用药品。 | ★★★ | |
| 2.会给物质加热。 | ★★★ | ||
| 3.会使用和连接简单仪器。 | ★★★ | ||
| 4.会检查装置气密性。 | ★★★ | ||
| 5.会过滤和蒸发。 | ★★★ | ||
| 6.会配制一定溶质的质量分数的溶液。 | ★★★ | ||
| 7.能安全操作,能处理一般意外事故。 | ★★ | ||
| 物质的制备和性质 | 气体的制取 | 能用简单装置和方法制取氧气和二氧化碳。 | ★★ |
| 物质性质的实验 | 1.能描述物质变化过程中的主要现象。 | ★★ | |
| 2.能测定空气中氧气的体积分数。 | ★★ | ||
| 3.能测定水的组成。 | ★★ | ||
| 4.能用一氧化碳还原氧化铁。 | ★★ | ||
| 5.能稀释浓硫酸。 | ★★ | ||
| 6.知道浓硫酸、浓盐酸、氢氧化钠等药品的保存方法。 | ★ | ||
| 物质的 检验与鉴别 分离与提纯 |
1.会检验氧气、二氧化碳和碳酸盐。 | ★★★ | |
| 2.能用过滤、蒸发的方法分离混合物。 | ★★ | ||
| 3.会依据物质的性质进行鉴别和提纯。 | ★★★ | ||
| 以上内容简单综合 | ★★★ | ||
重要知识点梳理:
(一)化学实验常用仪器的使用和基本操作
Ⅰ 化学实验常用仪器及使用(详见上册书附录)
Ⅱ 化学实验基本操作
1.试剂的取用
取用药品时,不能直接用手接触药品,不能尝任何药品,不能凑近容器口闻气味,闻气味时要扇闻。多取的药品不能放回原瓶,以防污染原试剂,需要放入指定容器。
(1)固体药品的取用
①往试管里装入固体粉末时,可先把试管横放,再把盛有药品的药匙或纸槽小心地送入试管底部,然后把试管直立,使药品全部落在试管底部,以免药品沾在管口或管壁上;
②往试管里装入块状药品或金属颗粒时,也应先把试管横放,再用镊子或药匙把药品放入试管里,然后把试管慢慢竖立起来,使药品缓缓地滑落到试管底部,以免打破试管;
③用过的药匙或镊子应立即用干净的纸擦拭干净;
④没有说明用量时一般取盖满试管底部即可。
(2)液体药品的取用
①瓶塞倒放在桌面上,倾倒液体时,试剂瓶的标签向手心;倾倒后,试剂瓶口应在试管口上轻刮一下,以免液滴沿着试剂瓶的外壁流下;
②没有说明用量时一般取1 mL~2 mL。
2.物质的称量
(1)托盘天平的使用程序
天平调零-----托盘垫纸(或小烧杯)-----左物右码(从大到小)-----平衡读数-----砝码回盒-----游码回零
(2)量筒的使用程序
量筒平放-----倒入液体-----平视刻度-----准确读数-----倒出液体-----洗净量筒
3.物质的加热
(1)加热前要将试管的外壁擦干,防止水滴附着受热不均匀,使试管破裂;
(2)加热固体时试管口稍向下倾斜,防止固体受热时产生的水蒸气冷凝回流引起试管炸裂;
(3)加热药品时先均匀加热,再集中加热有药品的部位;
(4)加热液体,也要进行预热,同时液体体积不要超过试管容积的1/3,试管与桌面成45°角,管口不得对人。
4.仪器的装备
实验装置的安排顺序从下到上,从左到右;制备气体时发生装置在左,收集装置在右,气流方向从左到右。连接中如需把玻璃导管插入带孔的橡皮塞时,应先将玻璃导管的一端用水润湿,再稍稍用力转动,使其插入;连接玻璃管和橡皮管时,也应先将玻璃管口润湿再稍稍用力插入;在玻璃容器口塞橡皮塞时,应转动着将橡皮塞慢慢塞入。
5.仪器的洗涤
少量水注入仪器中,经振荡或毛刷轻轻刷洗,再用清水冲洗几次即可。如果内壁有油脂,可使用热纯碱或洗衣粉洗涤。
玻璃仪器洗涤干净的标准是:水膜均匀,既不聚成水滴,也不成股流下。
6.装置气密性的检查

如图:将导管放入水中,形成密闭体系,用手捂住容器,
观察导管口是否有气泡产生,松手后是否有水进入导管到水面上一段距离。
7.气体的收集(如图)
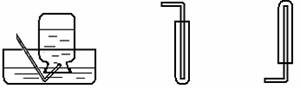
排水集气法 向上排空气法 向下排空气法
(1)溶于水或与水反应的气体不宜使用排水集气法收集;
(2)收集气体时如果气体的密度大于空气的密度,可以用向上排空气法收集,如氧气、二氧化碳;
(3)收集气体时如果气体的密度小于空气的密度,可以用向下排空气法收集,如氢气;
(4)使用排空气法用试管收集气体时,进入试管的导管要伸入试管底部,便于气体充满整个试管,同时便于空气的排除,并要进行验满。(用集气瓶收集时操作原理同上)
8.一定溶质质量分数溶液的配制
(1)计算:固体的质量或浓溶液的体积和水的体积;
(2)称量和量取:天平称量固体或量筒量取液体(粗略量取);
(3)溶解:加快固体溶解的方法是 研细固体、加热或搅拌。
具体操作过程如下图所示:

9.常见事故的处理
(1)浓硫酸溅到皮肤上,应立即用大量的水冲洗,并涂上3%~5%的碳酸氢钠溶液;不慎将酸溅到眼中,立即用水冲洗,边洗边眨眼睛,必要时请医生治疗;大量酸液洒到桌上,要加适量碳酸氢钠中和,然后用水冲洗,用抹布擦净;
(2)浓碱液溅到皮肤上,用较多的水冲洗后,涂抹硼酸溶液;大量碱液洒到桌上,要加适量醋酸中和;
(3)酒精灯不慎碰倒起火,用沙子或湿抹布盖灭,不能用水泼灭。
(二)物质的制备和性质
Ⅰ 气体的实验室制法
| 氧气 | 二氧化碳 | |
| 药品 | H2O2(MnO2)或KMnO4或 KClO3(MnO2) |
大理石和稀盐酸 |
| 反应原理 | 2H2O2 2KMnO4 |
CaCO3+2HCl |
| 仪器装置 | 固液不加热 固固加热  |
固液不加热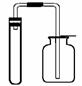 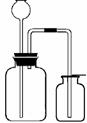 |
| 收集方法 | 排水法、向上排空气法 | 向上排空气法 |
| 验满 | 带火星木条靠近集气瓶口 | 燃着木条靠近集气瓶口 |
| 注意事项 | 若加热高锰酸钾制氧气,导管进气处应放一小团棉花,以防止高锰酸钾粉末随气体导出;排水法收集后,先撤导管后停止加热 |
Ⅱ 物质的性质实验
1.空气中氧气的体积分数的测定
2.能描述物质变化过程中的主要现象
物质性质的实验中,实验现象是复习的重点之一。对已学过的实验现象进行归纳、整理,有助于知识的掌握和应用。
(1)氧气、二氧化碳的化学性质实验
例如:碳、硫、磷、镁、铁丝、氢气、甲烷等在氧气中的燃烧;二氧化碳灭火、与水反应、与澄清石灰水反应等等。
(2)酸、碱、盐的化学性质实验
例如:
酸的化学性质的实验现象
| 盐 酸 | 稀 硫 酸 | |
| 紫色的石蕊溶液 | 溶液变为红色 | 溶液变为红色 |
| 活泼金属(锌) | 有无色气泡产生 | 有无色气泡产生 |
| 金属氧化物(锈铁钉) | 铁钉表面的锈被除去,溶液略带黄色 | 铁钉表面的锈被除去,溶液略带黄色 |
| 碱(氢氧化铜) | 蓝色固体溶解,溶液由无色变为蓝色 | 蓝色固体溶解,溶液由无色变为蓝色 |
| 氢 氧 化 钠 | 氢 氧 化 钙 | |
| 紫色的石蕊溶液 | 溶液变蓝 | 溶液变蓝 |
| 无色的酚酞溶液 | 溶液变红 | 溶液变红 |
| 酸性氧化物(CO2) | 气体被吸收,溶液无变化 | 气体被吸收,产生白色沉淀 |
| 盐(Na2CO3)溶液 | 无现象 | 产生白色沉淀 |
实验现象、实验结论等等。
4.一氧化碳的还原性
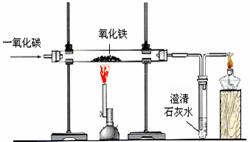
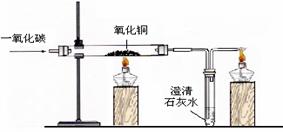
一氧化碳还原氧化铜 一氧化碳还原氧化铁
CuO+CO
 e+ 3CO2
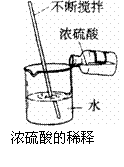
e+ 3CO25.浓硫酸的稀释
稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水中,
并不断搅拌。切不可将水倒进浓硫酸中。
6.常见物质的保存方法
①易见光分解的物质,需放入棕色瓶中,置于冷暗处,如过氧化氢溶液等;
②碱性溶液应用橡胶塞,而不用玻璃塞,如氢氧化钠溶液、碳酸钠溶液、澄清石灰水等;
③氢氧化钠、氧化钙、浓硫酸、浓盐酸需密封保存;
④白磷(少量保存在水里)。
(三)物质的鉴别和除杂、分离
Ⅰ 物质的检验与鉴别
1.氧气、二氧化碳、一氧化碳、甲烷的鉴别方法
2.几种重要的酸、碱、盐的检验
3.能用pH试纸和酸碱指示剂鉴别酸溶液和碱溶液。
II 混合物的分离
1.吸附、沉淀、过滤、蒸馏等方法可以不同程度的将水净化
2.粗盐提纯-----混合物的分离(溶解、过滤、蒸发)
III 除杂
除杂可以有多种方法,但不管采用什么方法,都应该遵循“不变,不引,好分”的基本原则。“不变”是指在除杂过程中不能将非杂质转化掉;“不引”是指在除杂过程中,不能引入新的杂质;“好分”是指除杂过程中新生成的物质应与原物质易于分离,如生成气体、沉淀等。常用的除杂方法有将杂质转化为气体、将杂质转化为沉淀、将杂质转化为有用的物质、将气体中的杂质吸收等几种。
第一、物理方法(1)溶解、过滤 例如:粗盐的提纯 (2)蒸馏
第二、化学方法
(1)将杂质变为气体除去。
(2)将杂质变为沉淀除去。
(3)转化杂质。
(4)洗气。
【例题解析】
为了除去Na2SO4溶液中含有的杂质Na2CO3 ,甲、乙、丙三位同学分别选用一种试剂(适量)进行实验。请你对他们所选用的试剂进行评价:
| 学生 | 选用试剂 | 评价(是否可行,并简述理由) |
| 甲 | HCl | |
| 乙 | H2SO4 | |
| 丙 | Ba(OH)2 |
【分析】本题是一道评价实验方案的题。题目针对要除去Na2SO4溶液中含有的杂质Na2CO3,给出三种实验方案,意在考察我们除去杂质的过程中是否遵循“不引,不变,好分,易行”的基本原则,并引导我们全面地分析问题,并能准确的简述理由。解题思路:分析甲学生加入试剂稀盐酸后,确实可把碳酸钠除去,但又引入新杂质氯化钠,且溶于水不好与硫酸钠分离,故不可行。乙同学加入试剂稀硫酸后,不但可与碳酸钠反应将除去,还可生成硫酸钠,且不引入新杂质。丙同学加入试剂氢氧化钡溶液后,它不但与杂质碳酸钠反应,还与主要物质硫酸钠反应,且引入新杂质氢氧化钠。今后我们在评价实验方案时应注意从以下几方面思考:原理正确、操作简便、现象明确、药品经济、节能环保、安全可靠。
【答案】
不行,除去Na2CO3的同时又引入了新杂质NaCl。
行,除去 Na2CO3 的同时增加了Na2SO4 而且没引入新杂质。
不行,除去Na2CO3 的同时也除去了Na2SO4 ,并引入了新杂质NaOH。
