| 考试内容 | 考试要求 | 目标层次 | |
| 空 气 和 水 |
空气 | 1.知道空气的主要成分。 | ★ |
| 2.认识空气对人类生活的重要作用。 | ★★ | ||
| 氧气 | 1.知道氧气的主要性质和用途。 | ★ | |
| 2.用氧气的性质解释一些常见的现象。 | ★★★ | ||
| 二氧化碳 | 1.知道二氧化碳的主要性质和用途。 | ★ | |
| 2.用二氧化碳的性质解释一些常见的现象。 | ★★★ | ||
| 水 | 1.认识水的组成。 | ★★ | |
| 2.知道纯水与矿泉水的区别。 | ★ | ||
| 3.认识水是宝贵的自然资源,有保护水资源和节约用水的意识。 | ★★ | ||
| 金属 与金 属矿 物 |
金属 | 1.了解金属的物理特征;认识金属材料在生产、生活和社会发展中重要作用。 | ★★ |
| 2.了解防止金属锈蚀的简单方法。 | ★★ | ||
| 3.知道生铁和钢是重要的合金。 | ★ | ||
| 4.知道废弃金属对环境的污染,及回收金属的重要性。 | ★ | ||
| 金属矿物 | 认识一氧化碳可以将铁矿石中的铁还原出来。 | ★★ | |
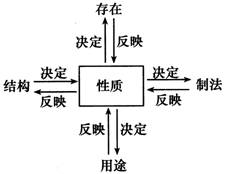
对身边的化学物质的认识包括该物质的结构、性质、制法、用途、检验、除杂、保存等。这些知识点之间并不是孤立的,而是一个有机整体。其中物质的性质,包括物理性质和化学性质是核心,是关键。系统复习一种物质一般可采用以下顺序进行:结构→性质→用途、存在、制法、检验,其内在联系可用下图表示。
空气和水
(一)空气
1.空气的成分:按体积计算,氮气78%,氧气21%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%,空气是混合物。
2.空气是一种宝贵的资源:
氧气:(1)供给呼吸:医疗急救、潜水、宇宙航行。
(2)支持燃烧;燃料燃烧、金属切割、气焊、炼钢、化工生产等。
氮气:化学性质不活泼,可用作保护气,防腐气;液氮创造低温环境,用于麻醉剂和超导材料;
还是制取硝酸和化肥的原料。
稀有气体:化学性质很稳定,可用作保护气;还可用作电光源,创造低温环境等。
3.大气污染的危害:严重损害人体的健康,影响作物的生长,破坏生态平衡,全球气候变暖、臭氧层破坏和酸雨等与空气污染有关;
保护大气:加强监测,使用清洁能源,植树造林等。
(二)氧气、二氧化碳的性质和用途
| 物质 | 物理性质 | 化学性质 | 用途 |
| 氧 气 O2 |
1.通常情况下,是无色、无味的气体,其固体和液体均为淡蓝色。 2.不易溶于水。 3.密度比空气略大。 (后两个性质决定了氧气的收集方法) |
氧气是一种化学性质比较活泼的气体,能与许多物质发生化学反应,在反应中提供氧,具有氧化性,是常用的氧化剂 与非金属反应:C+O2 S+O2 4P+5O2 2H2+O2 与金属反应:3Fe+2O2 2Mg+O2 与化合物反应:2CO+O2 CH4+2O2 |
(1)供呼吸。如高空飞行、潜水、登山等缺氧的场所,其工作人员都需要供氧;病人的急救。 (2)利用氧气支持燃烧并放热的性质,用于冶炼金属(吹氧炼钢)、金属的气焊和气割、作火箭发动机的助燃剂、制液氧炸药等。 |
| 二 氧 化 碳 CO2 |
1.通常状况下为无色无味气体,固态二氧化碳(干冰)会在-78.5℃以上直接气化并吸收大量的热; 2.密度比空气大;3.能溶于水。 (后两个性质决定了二氧化碳的收集方法) |
1.一般情况下,不能燃烧,不支持燃烧也不供呼吸。 2.与水反应生成碳酸: CO2+H2O=H2CO3 反应后的溶液使紫色石蕊试液变红。 3.与可溶性碱反应: CO2+Ca(OH)2=CaCO3↓+H2O 该反应用于检验二氧化碳。 CO2+2NaOH=Na2CO3+H2O 该反应用于吸收二氧化碳。 |
灭火、光合作用、气体肥料、化工产品的原料、用干冰进行人工降雨等。 温室效应:大气中的二氧化碳等气体过多,像温室的玻璃使地球变暖。造成冰川融化,海平面升高,土地沙漠化、农业减产等。应减少使用化石燃料、大量植树造林等。 |
| 自然界的二氧化碳与氧气的循环:动植物的呼吸、煤等化石燃料的燃烧都产生二氧化碳,而绿色植物的光合作用却吸收二氧化碳放出氧气。 | |||
(三)一氧化碳、甲烷
| 物质 | 物理性质 | 化学性质 | 用途 |
| 一 氧 化 碳 CO |
1.通常状况下为无色、无味气体; 2.密度比空气略小; 3.难溶于水。 |
1.可燃性 2CO + O2 点燃 2CO2 2.还原性:CO+ CuO 加热 Cu + CO2 3.毒性:一氧化碳易与血液中的血红蛋白结合,使人体因缺氧而死亡 |
气体燃料,冶金工业。 |
| 甲 烷 CH4 |
1.通常状况下为无色、无味气体; 2.难溶于水; 3.密度比空气小。 |
可燃性 CH4 +2O2点燃CO2 +2H2 O |
是沼气,天然气的主要成分,最简单的有机物,用作燃料。 |
(五)水
1.水的组成:由电解水生成氧气和氢气,氢气在氧气中燃烧生成水等实验都能证明水是由氢、氧两种元素组成的。
构成水的粒子是水分子,一个水分子是由两个氢原子和一个氧原子构成的。
2.自然界中的水:
纯水与天然水:纯水是无色、无臭、清澈透明的,构成粒子是水分子,是纯净物;天然水(例如矿泉水、河水、海水等)里含有许多可溶性和不溶性杂质,是混合物。
净化水的方法有吸附、沉淀、过滤、蒸馏等。
硬水与软水:含有较多可溶性钙、镁化合物的水叫硬水,不含或含较少可溶性钙、镁化合物的水叫软水。煮沸和蒸馏都可以软化水。
3.认识水是宝贵的自然资源,有保护水资源和节约用水的意识:
地球的总储水量大,但淡水很少。人类生活和生产用水量增大,工业、农业及生活对水体造成的污染造成水资源的危机。
爱护水资源一方面要节约用水,另一方面要防止水体污染。
金属与金属矿物
(一)金属的物理性质和用途
1.共性:常温下是固体、有金属光泽、大多为热和电的良导体(用作加热器具和导线),有延展性(能展成薄片、拉成丝)、密度大、硬度大、熔点高等共性,但导电性、导热性、密度、熔点、硬度等也会存在较大的差别。
2.特性:铁、铝等多数金属银白色,而铜为紫红色;多数为固态,而汞为液态等。
3.合金:在金属中加热熔合某些金属或非金属,就可以制得具有金属特征的合金。合金的强度、硬度和抗腐蚀性一般比组成它们的纯金属好,有更广泛的用途,生活中大量使用的不是纯金属而是合金,如生铁和钢;钛和钛合金等。
钢和生铁都是铁碳合金,生铁的含碳量为2%—4.3%,钢的含碳量为0.03%—2%。
4.金属的性质很大程度上决定了它们的用途,例如,制造飞机机翼的金属,需要坚硬而质轻;用于制造切割工具的金属,需要有很大的硬度;制造电灯丝的金属,熔点要高;制造保险丝的金属熔点要低;制造化工设备的金属要耐腐蚀等。但性质不是唯一的决定因素,还需要考虑价格、资源、是否美观、使用是否便利、废料是否易于回收和对环境的影响等。
(二)金属的化学性质
1.与氧气的反应:金属因活泼性不同,与氧气反应的难易和剧烈程度不同。
(1)镁、铝等在常温下(在空气中)就能与氧气反应。例:4Al+3O2=2Al2O3
银白色的铝的表面生成一层致密的氧化铝薄膜,因此,铝具有很好的抗腐蚀性能。
(2)
①铁在常温下的干燥空气中,很难与氧气发生反应,但在潮湿的空气中,铁与空气中的氧气和水蒸气共同作用会生成暗红色的疏松的铁锈(主要成分是Fe2O3·xH2O)。
②铁丝在氧气中点燃,会剧烈燃烧,火星四射,放出大量的热,生成黑色的四氧化三铁固体。
3Fe+2O2
(3)金在高温下也不与氧气反应。
2.与稀硫酸、盐酸反应生成相应的盐和氢气:
Mg+H2SO4=MgSO4+H2↑ Mg+2HCl= MgCl2+H2↑
Zn+H2SO4=ZnSO4+H2↑ Zn+2HCl=ZnCl2+H2↑
Fe+H2SO4=FeSO4+H2↑ Fe+2HCl=FeCl2+H2↑
3.与某些盐溶液反应生成另一种盐和另一种金属:
Fe+CuSO4
2Al+3CuSO4
Cu+2AgNO3
金属与稀盐酸、稀硫酸及与盐溶液反应能否发生都取决于金属在金属活动顺序表中的位置。

a.在金属活动顺序表中位于氢前的金属能把稀盐酸、稀硫酸中的氢元素置换出来。
b.在金属活动顺序表中位置靠前的金属(K、Ca、Na除外)能把位置靠后的金属从它的盐溶液中置换出来。
(三)铁的冶炼
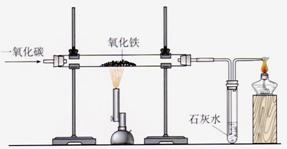
主要反应原理:在高温下,一氧化碳夺取铁矿石里氧化铁中的氧,将铁还原出来:
Fe2O3+3CO
(四)金属资源的保护
1.铁的锈蚀和防护:因为铁的锈蚀条件是铁与空气和水接触,所以防止铁制品锈蚀的方法是破坏铁锈蚀的条件。如:在钢铁表面涂油、刷漆、镀耐磨和耐腐蚀的铬及制造耐腐蚀的合金(如不锈钢)等。
2.金属资源的保护主要包括;防止金属锈蚀;金属回收利用;合理开采矿物;寻找金属替代品等。
【例题解析】
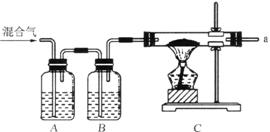
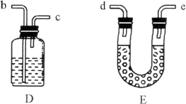
水煤气的主要成分是CO和H2,还含有少量的CO2和水蒸气。为验证水煤气的主要成分是CO和H2,采用下图所示装置,各装置中可供选择的试剂是:①澄清的石灰水,②NaOH溶液,③浓硫酸,④氧化铜,⑤无水CuSO4固体。
(1)B、C装置中盛有的试剂是B________,C________;
(2)将装置连接完整(填字母),a接________,________接________;
(3)写出装置D中所发生反应的化学方程式________________。
[答案]
(1)B浓硫酸 C氧化铜
(2)a接d(或e) e(或d)接b
(3)CO2+Ca(OH)2==CaCO3↓+H2O
[解析]
利用CO和H2与CuO的反应,可说明它们的存在。 CO和H2与CuO反应,除了生成Cu外,还分别生成CO2和H2O。若证明有CO2和H2O生成,即可证明有CO和H2的存在。又因为混合气体中含有少量CO2和水蒸气,它们的存在会对CO和H2的检验产生干扰。因此,在气体通入灼热的CuO之前,必须先将其除去。尽管NaOH的溶液和Ca(OH)2溶液都可吸收CO2,但NaOH溶液吸收的更充分,所以要用NaOH溶液吸收CO2,且吸收CO2要在除去水蒸气之前(因为混合气体通入NaOH水溶液时,有可能再带出水蒸气)。因此,对水的检验和除杂可以概括为“验水先验,除水后除”。
