A.原子是最小的粒子,不可再分
B.钠原子的质子数大于钠离子的质子数
C.当二氧化碳气体变成干冰时,二氧化碳分子间不存在间隔
D.分子、原子、离子都可以直接构成物质
2.今年4月19日,温家宝总理批示:严查安徽“杀人奶粉”。经检测“杀人奶粉”中蛋白质、钙、磷、锌、铁等的含量严重不足,营养价值比米汤还差。这里的钙是指
A.原子 B.分子 C.元素 D.单质
3.科学家用计算机模拟确认,60个N原子可结合成一个N60分子。下列 叙述中正确的是
A.N60是一种新型的化合物 B.一个N60分子中含有30个N2分子
C.N60和N2的性质完全相同 D.N60和N2混合后形成的是混合物
4.右图为某加碘食盐包装袋上的部分内容,你从中得到的信息看,下列判断正
 确的是
确的是A.该食盐是纯净物
B.加碘食盐中的碘是指碘单质
C.碘酸钾受热不稳定
D.1kg食盐中含碘酸钾(35±15)mg
5.常温下,有些盐如CaCl2、NaCl等物质的水溶液呈中性;有些盐如Na2CO3等物质的水溶液呈碱性;有些盐如NH4Cl等物质的水溶液呈酸性。现有HCl与CaCl2的混合溶液,向其中逐滴加入过量某
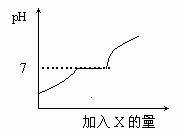 物质X,溶液的pH随滴入X的量的变化关系如右图所示。则X是
物质X,溶液的pH随滴入X的量的变化关系如右图所示。则X是 A.水
B.澄清石灰水
C.纯碱溶液
D.稀盐酸
6.水果尤其是猕猴桃中含有丰富的维生素C,多吃水果可以预防坏血病。下列关于维生素C(C6H8O6)的说法中,不正确的是
A.维生素C由三种元素组成
B.维生素C是由20个原子构成的
C.维生素C中碳、氢、氧元素的质量比为9∶1∶12
D.一个维生素C分子中,碳、氢、氧原子的个数比为3∶4∶3
7.2008年9月27日,我国航天员翟志刚进行了首次太空行走。在此次活动中需要“人造空气”来供航天员呼吸,这种“人造空气”中含有体积分数为70%的氮气、20%以上的氧气、还有二氧化碳。下列关于“人造空气”的说法中,不正确的是
A.“人造空气”比空气中的氮气含量低
B.“人造空气”中供给航天员呼吸的是氧气
C.“人造空气”中的氧气和空气中的氧气化学性质相同
D.氮气对航天员呼吸没有任何作用,因此“人造空气”可以不需要氮气
8.经测定,某含有碳、氧两种元素组成的混合气体中,碳元素的质量分数为30%,则混合气体中一定含有的是
A.氧气
B.一氧化碳
C.二氧化碳
D.二氧化碳和一氧化碳
9.生物课中我们学过淀粉溶液遇碘会变成蓝色。实验表明,无论是固体碘还是碘蒸气,均能使淀粉溶液变蓝色。这一现象说明( )。
A.同种分子质量相等 B.同种分子体积相等
C.同种分子化学性质相同 D.同种分子运动速度相同
10.已知H2能在O2、Cl2中燃烧生成H2O、HCl。右图中横坐标表示完全燃烧时消耗气体X(X = A、B、C)的分子数n(x),纵坐标表示消耗H2的分子数n(H2)。已知A、B是纯净物,C是由A和
 B组成的混合物,则C中n(A) ∶n(B)为( )。
B组成的混合物,则C中n(A) ∶n(B)为( )。A.2∶1
B.1∶1
C.2∶3
D.2∶5
11.已知某物质X是一种消毒杀菌效率高、二次污染小的水处理剂,又知该物质的制备原理为2KClO3 + 4HCl(浓) =2KCl + 2X + Cl2↑+2H2O。则X的化学式为
A.ClO2 B.HClO C.Cl2O5 D.HClO3
12.在实验室易燃品橱柜里有一瓶失去标签的试剂,某同学为探究其成分,进行如下实验分析:取2.16 g该物质,使其充分燃烧,测知只生成2.16 g水和5.28 g二氧化碳。请你通过计算填空:
(1)该物质中含氢元素__________g, 含碳元素__________g
(2)该物质中__________(填“含”或“不含”)有氧元素;若含有氧元素,其质量为__________g (若不含氧元素,此空不填)。
(3)某同学据推测该物质可能是酒精,你认为这个推测合理吗?__________,说明理由__________。
13.(09海淀一模)20℃时,将等质量的甲、乙两种固体,分别加入盛有10g水的A、B试管中,充分溶解后,可观察到如图所示的现象,甲、乙的溶解度曲线如右图所示。
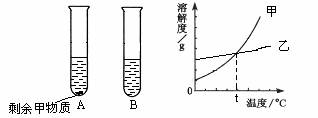
(1)在A、B试管的溶液中,水作__________,20℃时,(填“A”或“B”)__________试管中,一定是饱和溶液。
(2)若要使A试管中剩余的甲物质继续溶解,可采取的方法有(填两种方法)__________。
(3)若温度在t℃以上,有质量相同的甲、乙两饱和溶液,降温到20℃,(填“甲”或“乙”) _____________析出的晶体多。
(4)20℃时,对A试管进行如下操作,最终A试管中溶液的溶质质量分数一定发生变化的是(填序号)__________。
① 升温到40℃ ② 加入少量甲物质
③ 加少量水 ④ 蒸发部分溶剂,恢复到20℃
⑤ 加入少量40℃时的甲的饱和溶液,恢复到20℃
【参考答案】
1、D 2、C 3、D 4、C 5、C
6、B 7、D 8、B 9、C 10、D 11、A
12.(1)0.24 1.44
(2)含 0.48
(3)不合理 酒精中C∶H∶O质量比为12∶3∶8,而该物质中C∶H∶O质量比为6∶1∶2
13.(1)溶剂 A
(2)加水、加热
(3)甲
(4)①
