类型一(以物质色态、用途为突破口)
知识点梳理:
总结归纳常见物质的颜色,并填写下表。(西城区总复习)
| 颜色 | 物质 |
| 黑色 | C 二氧化锰 四氧化三铁 氧化铜 铁粉 |
| 红色 | 铜 氧化铁 红磷(暗红) 酸与紫色石蕊 碱与酚酞 |
| 黄色 | S 含Fe3+的溶液 |
| 蓝色 | 含Cu2+的溶液 氢氧化铜 碱与紫色石蕊 |
| 浅绿色 | 含Fe2+的溶液 |
| 紫色 | 紫色石蕊 紫红色溶液:高锰酸钾溶液 暗紫色固体:高锰酸钾 |
| 备注 | 除上述物质外,其他金属多为银白色,固体多为白色,其溶液多为无色 |
总结典型物质的用途
1.______________用于急救病人。________________用于提高炼钢炉温。
2.______________用于灭火,______________用于人工降雨, ____________用于光合作用。
3.________________用于高能燃料,最理想的燃料。
4._______________用作气体燃料,(其中______________有毒,_______________无污染)。
5.________________称为三大矿物燃料。
6.________________用作干燥剂。
7.________________用于金属除锈。
8.________________常用作食品“双吸剂” 。
9.____________常用作改良酸性土壤。_________常用作改良碱性土壤,同时可以_________。
10.________________可用于治疗胃酸过多。
11.________________是重要调味品,配制生理盐水。
12.________________广泛用于玻璃、洗涤剂等的生产。
13.________________广泛用于肥皂、石油等工业。
14.________________大量用于建筑业。
答案:
1. O2;O2 2. H2O,CO2; 干冰;CO2
3.H2 4. H2、CO、CH4 CO H2
5. 煤、石油、天然气 6. 浓硫酸、氯化钙固体、氢氧化钠固体、生石灰
7. 稀盐酸、稀硫酸 8. 还原铁粉
9. Ca(OH)2 , 碳酸水 促进植物光合作用 10. 碳酸钠、氢氧化铝
11. 氯化钠 12. 碳酸钠
13. 氢氧化钠 14. 碳酸钙、氢氧化钙
1.(昌平一模)小华取回该公司换下的旧铁质管道内的铁锈样品A,进行如下图所示的相互转化研究:已知B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应。你来完成他的研究过程:

(1)写出反应②的化学方程式________________。
C的固体俗称________________;该物质可用做________________。
(2)写出X溶液中溶质的化学式________________。
(3)写出反应③中生成红色固体的化学方程式________________。
2.(大兴一模)甲、乙、丙三种物质可发生如下图所示的变化(③为分解反应)。
 |
|
①________________ ②________________ ③________________
(2)若乙的水溶液为蓝色,写出反应①、②、③的化学方程式。
①________________ ②________________ ③________________
3.(崇文二模)在一定条件下,下列物质可实现如下转化(反应条件已略去)。其中有两种物质是单质,G的溶液为浅绿色。另从查阅资料可知,铁与高价铁盐溶液反应,生成亚铁盐溶液,如:2FeCl3+Fe=3FeCl2 。
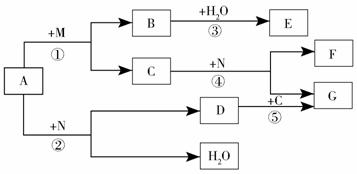
试回答:
(1)C的化学式为_____________,F的化学式为______________,M的化学式为____________。
(2)反应②的化学方程式为________________。
(3)反应③的化学方程式为________________。
(4)反应④的化学方程式为________________。
4.(宣武一模)(6分)A、B、C、D、E、F是初中化学中常见的物质,A是暗紫色固体,B为黑色固体。请根据图中物质间的相互转化关系,回答有关问题:
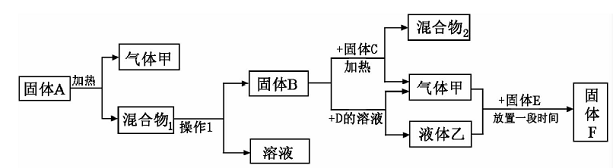
(1)检验气体甲的方法是________________。
(2)在加热固体C中,固体B起________________作用。
(3)操作1的步骤是________________,所需使用的仪器有________________。
(4)写出加热固体A的化学方程式:________________。
(5)固体F含有的物质可能是________________。(填化学式)
类型二(以反应条件为突破口)
1.下图是一定条件下相关物质的转化关系,其中A是只含两种元素的纯净物,B、C、E、F均是初中常见的无色、无味的单一气体。
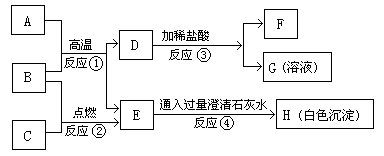
(1)写出下列物质的化学式C:______;E:_______;F:______ H:________。
(2)写出符合反应①的一个化学反应方程式:___________________。
2.已知A、B、C、D四种物质都含有同一种元素,其中A是单质,B是黑色固体,C是红色固体。它们之间存在着如下转化关系:
(1)A在不同条件下能够转化成B或C;
(2)A和稀硫酸反应有D生成;
(3)在高温条件下,B、C分别和无色气体E反应,都能生成A和另一种无色气体。
根据上述信息,写出下列物质的化学式:
A ___________ ; C ____________ ; D ____________; E _____________。
3.A为含三种元素的钠盐,C为相对分子质量为100白色不溶物,请填空:
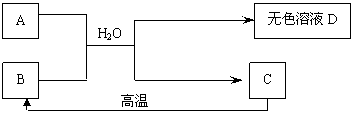
(1)A________________、B________________、C________________。(填写化学式)
(2)D中一定含有的溶质是_____________。理由是(用化学方程式表示)_______________。
(3)D还可能含有溶质是________________。
类型三(以反应类型为突破口)
1.右图中的各物质均为初中化学常见物质。请根据图示
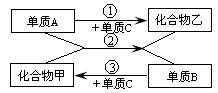 关系回答:
关系回答:(1)甲物质的元素共有________________种;
(2)反应②的基本反应类型为________________;
(3)若常温下乙为无色液体,则A为________________;
反应②的化学方程式可能为________________。
2.(丰台一模)以下是一些常见物质的相互转化关系图,其中甲、乙均属于盐类(有些条件已省略)。
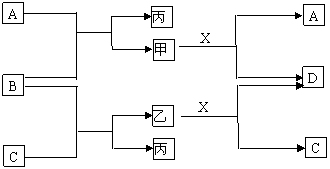
请根据上图填空:
(1)若反应全部为置换反应,写出B、D两种物质的化学式:B___________,D_________;生成甲的化学反应方程式为________________;
(2)若反应全部为复分解反应,写出B、D两种物质的化学式:B__________,D___________;生成甲的化学反应方程式为________________。
 3.(西城二模)下图是初中化学中常见的六种物质之间的转化关系,其中A、B为化合物,另外四种物质皆为单质,四种单质中有三种是金属单质,且只有一种可以与稀盐酸发生置换反应。请回答:
3.(西城二模)下图是初中化学中常见的六种物质之间的转化关系,其中A、B为化合物,另外四种物质皆为单质,四种单质中有三种是金属单质,且只有一种可以与稀盐酸发生置换反应。请回答:(1)能与盐酸反应的金属是_______(写编号),其化学式为__________;
(2)D→F的化学方程式为_______________________________________;
(3)B→D的化学方程式为_______________________________________;
(4)实验室制备A的化学方程式为_________________________________。
4.(08西城1模)A、B、C、D、X为初中常见的物质,其转化关系如右图所示:
(1)若A、D为单质,其余均为化合物,则反应②的基本反应类型为__________,反
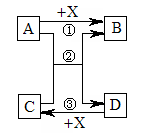 应的化学方程式为__________________。
应的化学方程式为__________________。(2)若A、B、C均为氧化物,则气体X为_______________,反应②的化学方程式为_____________________________。
(3)若A、B、C、D各含有三种元素,它们与X共同含有一种地壳中含量最多的元素,则反应②的化学方程式为___________。
类型四(物质之间的相互转化关系综合)
物质之间的相互转化关系小结:
1.H2O
1)H2O
 H2 2) H2O
H2 2) H2O  O2 3) H2O
O2 3) H2O  H2CO3 4) H2O
H2CO3 4) H2O  Ca(OH)2
Ca(OH)22.CO2
1)CO2
 CO 2)CO2
CO 2)CO2  H2CO3 3)CO2
H2CO3 3)CO2  CaCO3 4)CO2
CaCO3 4)CO2  Na2CO3
Na2CO33.金属和金属氧化物、金属和盐溶液
1)Fe
 Fe2O3 2)Fe
Fe2O3 2)Fe  Fe3O4
Fe3O43)Fe
 FeSO4 / FeCl2 / Fe(NO3)2 4) Cu
FeSO4 / FeCl2 / Fe(NO3)2 4) Cu  CuO
CuO4.酸、碱、盐NaOH
 Na2CO3
Na2CO31.(06北京中考)甲、乙、丙是初中化学中常见的物质,其转化关系如下图所示:

(1)若甲、乙组成元素相同,甲、乙、丙中有一种物质为水,则甲为(填化学式)____________;实验室制丙的化学方程式为_______________(写出一种)。
(2)若甲、乙、丙都含有三种元素,甲、乙、丙的相对分子质量依次增大,其中一种物质广泛用于玻璃、造纸、纺织和洗涤剂的生产。由甲到乙反应的化学方程式为________________。乙也可以转化成甲,其反应方程式为________________。
(3)若甲、乙、丙都含有三种元素,其中两种元素的质量比均为1∶2。图示反应中,一个有难溶物生成,另一个有气体生成,第三个有难溶物和水生成。
则生成气体可能为(填化学式)________________;丙为(填化学式)________________。
2.(朝阳二模)A、B、C均为初中化学常见物质,且有如图所示的转化关系。
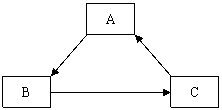
(1)A既能与生石灰反应又能与二氧化碳反应,C为铁锈的主要成分,则B物质的化学式为__________,C→A的化学方程式为______________。
(2)A与碱溶液反应可生成B或C,且B也能与碱溶液反应生成C,则A物质的化学式为__________,B→C的化学方程式为_______________。
3.(宣武二模)现有甲、乙两种物质,它们都是初中化学中常见物质。在一定条件下甲可以转化为乙,乙也可转化为甲(如图,反应条件、其他生成物略去),请你按要
 求填写:(填出一种可能情况即可)
求填写:(填出一种可能情况即可)(1)甲为单质,乙为氧化物,则甲____________,乙______________。
(2)甲含两种元素,乙含三种元素,则甲____________,乙___________。
(3)甲、乙均含三种元素,甲、乙均广泛用在造纸、纺织等工业上,乙中三种元素原子个数比为2∶1∶3
写出甲转化为乙的化学方程式________________;
写出乙转化为甲的化学方程式________________。
类型五(以物质的化学性质为突破口)
典型物质的化学性质小结:
O2 Fe H2O CO2 Fe2O3 HCl和H2SO4 NaOH和Ca(OH)2 Na2CO3和CaCO3
1.(东城一模)对物质进行正确的分类,根据各类物质的性质寻找它们之间的反
 应关系,是学习化学知识的重要方法。
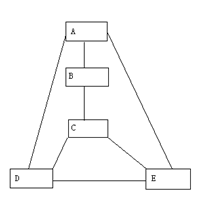
应关系,是学习化学知识的重要方法。(1)请选择适当的物质填入下图的方框内,使图中直线相连的物
质间能发生反应,要求所选物质必须分别属于“金属、非金属、氧化物、酸、碱、盐”六种类别中的四种类别。
(2)根据你所填写的物质,请写出其中D与E之间发生反应的化学方程式________________;该反应属于________________反应(填写基本反应类型)
2.(08西城2模)请从单质、氧化物、酸、碱、盐五类物质中分别选出一种初中常见的物质,使它们之间符合如下图所示的关系(图中“—”表示两端的
 物质能发生化学反应;“→”表示物质间存在转化关系;其中A、B、C、D、E的相对分子质量依次增大)。
物质能发生化学反应;“→”表示物质间存在转化关系;其中A、B、C、D、E的相对分子质量依次增大)。 (1)A的化学式为____________________,
D物质属于______________(填物质类别)。
(2)写出图中①②③反应的化学方程式:
①__________________________________________;
②__________________________________________;
③__________________________________________。
3.(昌平二模)酸、碱、盐溶解性表是学习化学的重要工具。下表为部分酸、碱、盐在水中的溶解性(20℃)。试回答:
| Ba2+ | Ca2+ | Mg2+ | Zn2+ | Fe2+ | Cu2+ | Ag+ | |
| OH– | 溶 | 微 | 不 | 不 | 不 | 不 | —— |
| SO42– | 不 | 微 | 溶 | 溶 | 溶 | 溶 | 微 |
| CO32– | 不 | 不 | 微 | 不 | 不 | 不 | 不 |
| Cl– | 溶 | 溶 | 溶 | 溶 | 溶 | 溶 | 不 |
________________。
(2)有A、B、C、D四种物质的稀溶液,右图为常温时上述溶液两两混合的实验
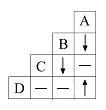 现象,其中“↓”表示生成沉淀,“↑”表示生成气体,“-”表示无明显现象或生成微溶物。请你结合上表,将推断的可能情况填写出来。
现象,其中“↓”表示生成沉淀,“↑”表示生成气体,“-”表示无明显现象或生成微溶物。请你结合上表,将推断的可能情况填写出来。① 写出A、D的化学式:A________________、C________________;
② B可能是________________。
③ 写出A和D反应的化学方程式________________。
类型一
1.
(1)Fe2O3+3CO
(2)CuSO4 , H2SO4
(3)Fe+CuSO4=Cu+Fe SO4
2.
(1) CaO+H2O=Ca(OH)2 Ca(OH)2+CO2=CaCO3↓+H2O
CaCO3
(2) CuO+H2SO4=CuSO4+H2O CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
Cu(OH)2
3.
(1) Fe H2 CO
(2) Fe2O3+6HCl=2FeCl3+3H2O
(3) CO2+H2O=H2CO3
(4) Fe+2HCl=FeCl2+H2↑
4.
(1)将带火星的木条伸入装有此气体的集气瓶中。
(2)催化
(3)溶解 过滤 , 烧杯 玻璃棒 漏斗 铁架台含铁圈 药匙
(4)2KMnO4
(5) Fe2O3 Fe
类型二
1.
(1) O2 CO2 H2 CaCO3 Fe2O3+3CO
2. Fe Fe2O3 Fe2SO4 CO
3.
(1) NaCO3 CaO CaCO3
(2) NaOH CaO+H2O= Ca(OH)2 Ca(OH)2+Na2CO3= CaCO3↓+2NaOH
(3) Na2CO3 或 Ca(OH)2
类型三
1
(1)2
(2)置换反应
(3)H2 H2+CuO
2.
(1) H2SO4 MgSO4 Fe+H2SO4==FeSO4+H2↑
(2) H2SO4 BaSO4 2NaOH +H2SO4==Na2SO4+2H2O
3.
(1) D Fe
(2) Fe+2AgNO3=2Ag+Fe(NO3)2
(3) 3CO+Fe2O3
(4) CaCO3+2HCl=CaCl2+H2O+CO2↑
4.
(1) 置换反应 H2+CuO
(2) CO2 4CO+Fe3O4
(3) Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
类型四
1.
(1) H2O2 2H2O
(2) CO2+2NaOH=NaCO3+H2O Na2 CO3+Ca(OH)2=CaCO3↓+2NaOH
(3) H2或CO2 BaSO4
2.
(1) O2 Fe2O3+3H2
(2) CO2 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
3.
(1) H2 H2O
(2) H2O H2CO3
(3) 2NaOH+CO2=Na2CO3+H2O Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
类型五
1.
(1) A→HCl B→Fe ,Fe2O3 C→H2SO4 D→Ca(OH)2 E→Na2CO3
(2) Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 复分解
2.
(1)HCL 金属氧化物
(2) 1)2HCl + Fe = FeCl2+H2↑
2) Fe+CuSO4=Cu+FeSO4
3) 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
3.
(1) Ba(OH)2+MgSO4=BaSO4↓+Mg(OH)2↓
(2) 1) Na2CO3 HCl
2) Ca(OH)2
2) 2HCl+Na2CO3=2NaCl+H2O+CO2↑
