1.“20℃时,氯化钾的溶解度为51g”的含义是
A.20℃时,氯化钾在水中最多能溶解51g
B.51g氯化钾溶解到100g水中便到达饱和
C.20℃时,在100g水中最多能溶解51g氯化钾
D.20℃时,51g氯化钾溶解到100g水中得到的是氯化钾的不饱和溶液
2.20℃时100g水中最多能溶解5g A物质;30℃时100g水中最多能溶解10g B物质,则A、B溶解度的大小关系为
A.SA>SB B.SA<SB C. SA=SB D.无法判断
3.在饱和石灰水中加入少量的生石灰,溶质的质量将会
A.增加 B.不变 C.减小 D.无法判断
4.25℃时,向100g质量分数为26.5%的NaCl饱和溶液中加入5gNaCl粉末,溶液中NaCl的质量分数将
A.增大 B.不变 C.减小 D. 无法判断
5.下图各点中表示某温度下的不饱和溶液的点是

6.在室温下,A、B、C三支试管中分别加入KNO3、NaCl、Ca(OH)2的饱和溶液,并有少
 量的固体存在(如图所示)。若使A、B试管中的固体增加,C试管中的固体减少或消失,应向试管外的烧杯中加入的物质是
量的固体存在(如图所示)。若使A、B试管中的固体增加,C试管中的固体减少或消失,应向试管外的烧杯中加入的物质是A.硝酸铵 B.石灰石
C.浓硫酸 D.氢氧化钠
7.取70g某温度下的氯化钾饱和溶液,将其恒温蒸发10g水,析出4g氯化钾固体,则剩余溶液中所含溶质质量为
A.16g B.20g C.40g D.56g
8.将100 g不饱和食盐水恒温蒸发水,直到有少量的晶体析出,在此过程中溶质的质量分数(ω%)与时间(t)的变化关系,下列图像中描述正确的是
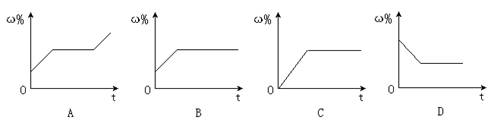
9.某实验小组要配制溶质的质量分数一定的食盐水,下列操作会导致溶质的质量分数变大的是
A.托盘天平没有调好,指针向右偏就进行称量 B.配制溶液的烧杯不干燥,留有少量的水
C.配好的溶液不慎洒了一部分 D.量取溶剂水时,仰视进行读数
10.在溶质质量分数为5%的氯化钠溶液中,再加入5 g氯化钠和95 g水,所得溶液的溶质的质量分数为
A.5% B.15% C.20% D. 无法判断
11.在25℃时向100gKNO3饱和溶液中加入1g NaCl固体,下列叙述不正确的是
A.NaCl固体不能溶解 B.加入的1gNaCl固体能溶解
C.所得溶液的质量是100g D.溶液中溶剂的质量不变
12.现有W克溶质的质量分数为15%的A溶液,欲使其溶质的质量分数增至30%,可采取的方法有
A.蒸发掉溶剂的二分之一 B.蒸发掉0.5Wg溶剂
C.加入0.15WgA D.加入3gA
13.据《说文解字》记载,我们的祖先在神农氏时代就开始利用海水晒盐。海水晒盐的原理是
A.日晒风吹使海水中的氯化钠蒸发
B.日晒风吹使溶液由饱和变为不饱和
C.日晒风吹使水分蒸发晶体析出
D.日晒风吹使氯化钠的溶解度变小
14.下列操作不会改变溶液中溶质的质量分数的是
A.对不饱和溶液蒸发溶剂(无晶体析出)
B.对硝酸钾溶液降温有晶体析出
C.对饱和硝酸钾溶液降温
D.对某固体物质的饱和溶液恒温蒸发溶剂
二、填空题
1.右图是A、B、C三种物质的溶解度曲线,据图回答:
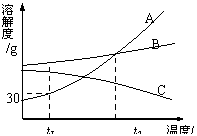
(1) t1℃时A、B、C三种物质的溶解度由大到小的顺序是______(填写序号,下同)。
(2) t1℃时30gA物质加入到50g水中不断搅拌,形成的溶液质量是_____g。
(3) 将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大小关系是____________。
2.右图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲
 线。
线。(1)当温度为10℃时,碳酸钠的溶解度为______;
(2)当温度 时,氯化钠的溶解度大于碳酸钠的溶解度;
(3)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”。
请你解释原因:“夏天晒盐”________________________;
“冬天捞碱”________________________。
请你解释原因:“夏天晒盐”________________________。
3.过氧乙酸是一种常用消毒剂,具有强氧化能力,可将各种病原微生物杀灭,广泛应用于公共场合的杀菌等。工业品过氧乙酸原液通常是15%的过氧乙酸(密度1.15 g/cm3)。使用时,通常取20mL原液,加自来水稀释至1000mL,搅拌均匀,即配制成1000mL(密度约为1g/cm3)用于空气喷雾消毒、环境地面消毒的过氧乙酸溶液。
⑴20mL15%的过氧乙酸原液的质量是多少克?其中含过氧乙酸多少克?
⑵配制成的1000mL过氧乙酸溶液中,过氧乙酸的质量分数是多少?
参考答案
一、选择题
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 答案 | C | D | C | B | C | A | A | B | A | A | B | B | C | D |
二、填空题
1.
(1) S(B)>S(C)>S(A)(或B、C、A或BCA);
(2) 65;
(3) B>C>A(或B、C、A或BCA)
2.
(1)10g
(2)大于等于0℃且小于30℃
(3)氯化钠的溶解度受温度影响不大,夏天温度高水分蒸发快,氯化钠易结晶析出;碳酸钠的溶解度受温度影响大,冬天温度低,碳酸钠易结晶析出。
3.8.⑴23g ;3.45g ⑵0.345%
