分子和原子 原子的构成
【知识要点】
构成物质的粒子有:分子、原子和离子
一.分子和原子
1.分子
(1)分子的特点:
① 小。分子质量和体积非常小,一滴水约有15万亿亿个水分子。分子虽然看不见也摸不着,但可以用扫描隧道显微镜拍摄出某些分子的照片,证明它真实存在着。


② 总是不停地做无规则运动。大量的生活事实,如我们能闻到花的香味、湿衣服会晾干、糖放入水中会溶解等,所有这些事实,都会使我们感受到分子的存在和总在不断运动着。分子的运动速率和温度有关,温度越高,物质的能量越大,分子的运动速率越大。如:100℃时,氢分子的平均速率能达1.987 km/s。气体分子的相互碰撞的次数是受条件影响的,压强大了,分子挤在一起,碰撞次数多;分子轻,分子的运动速率大,碰撞次数也多。据推算,标准状况下,每秒钟每个氢分子可能碰撞150亿次。
③ 分子之间存在空隙。物质呈三态变化的原因:分子之间的间隔大小发生变化的缘故。“等体积的水和酒精混合”,体积减小也是由于分子间存在间隔的原因。
④ 同种分子化学性质相同,不同种分子化学性质不同。
(2)分子的定义:
分子是保持物质化学性质的最小粒子。
说明:①单个分子不能保持物质的物理性质;②此定义只适用于由分子构成的物质。
(3)用分子的观点解释一些概念:
①物理变化:分子本身不变,改变的是分子之间的距离。
②化学变化:分子的本身发生了改变,生成了新的分子。
③纯净物:由一种分子构成的物质。
④混合物:由多种分子构成的物质。
2.原子
(1)定义:原子是化学变化中的最小粒子(或原子在化学变化中不能再分)
(2)化学变化的实质:分子被破坏,原子重新组合。
3.粒子构成物质的方式:
(1)
例如:水是由大量的水分子构成的,一个水分子是由二个氢原子和一个氧原子构成的。
氧气是由大量的氧分子构成的,一个氧分子是由二个氧原子构成的。
(2)原子
例如:①金属 ②稀有气体 ③金刚石(C)、石墨(C)、硅(Si)等
如:金属铁是由铁原子直接构成的。
附录:分子、原子的相似、相异及相互关系
| 原子 | 分子 | 备注 | |
| 概念 | 化学变化中的最小粒子 | 保持物质化学性质的最小粒子。 | 原子一定比分子小吗? |
| 相似性 | 小,轻,有间隔。 同种原子性质相同; 不同种原子性质不同; |
小,轻,有间隔。 同种分子性质相同; 不同种分子性质不同; |
|
| 相异性 | 在化学反应中不能再分。 | 在化学反应中,分裂成原子,由原子重新组合成新的分子。 | |
| 相互 关系 |
原子可以构成分子,由分子构成物质。如:氧气、氮气等。 原子也可以直接构成物质。 如:金属单质 |
分子是由原子构成的。 无数个同种分子构成物质。 |
构成物质的粒子有几种? |
二、原子的构成
1.原子的内部结构:


并不是所有的原子都是由这三种粒子构成的。如有一种氢原子中只有质子和电子,没有中子。
2.原子内部粒子的电性及电量:
质子:1个质子带1个单位正电荷;中子:不带电;电子:1个电子带1个单位负电荷。
而在原子中,原子核所带的正电荷数(核电荷数)就是质子所带的电荷数(中子不带电),而每个质子带1
个单位正电荷,因此,核电荷数=质子数,由于原子核内质子数与核外电子数相等,
所以在原子中:核电荷数=质子数=核外电子数=原子序数。
3.原子不显电性的原因:
原子是由居于原子中心带正电的原子核和核外带负电的电子构成,原子核又是由质子和中子构成,质子带正电,中子不带电;原子核所带正电荷(核电荷数)和核外电子所带负电荷相等,但电性相反,所以整个原子不显电性。
三.相对原子质量
1.标准:
碳-12 原子质量的1/12 (含6个质子和6个中子的碳原子,它的质量的1/12约等于1.66×10-27 kg。)
2.计算方法:
一种原子的真实质量比上碳-12 原子质量的1/12 ,所得的比值就是该原子的相对原子质量。
注意:
(1)相对原子质量只是一个比值,不是原子的实际质量,单位为“1”。
(2)相对原子质量不是一个原子的真实质量,但是可以根据其大小来判断不同原子之间真实质量的大小。
3.相对原子质量的近似处理:
构成原子的粒子有质子、中子、电子,1个质子和1个中子的质量都约等于1个电子质量的1836倍,跟相对原子质量的标准(即一个碳-12原子质量的1/12)相比,均约等于1,电子质量很小,跟质子和中子相比可以忽略不计,所以原子的质量主要集中在原子核上,故:相对原子质量≈质子数+中子数。
几种原子的构成:
| 原子种类 | 质子数 | 中子数 | 核外电子数 | 核电荷数 | 相对原子质量 |
| 氢 | 1 | 0 | 1 | 1 | 1 |
| 碳 | 6 | 6 | 6 | 6 | 12 |
| 氧 | 8 | 8 | 8 | 8 | 16 |
| 钠 | 11 | 12 | 11 | 11 | 23 |
| 氯 | 17 | 18 | 17 | 17 | 35 |
4.如何查阅相对原子质量:
(1)四舍五入法(取整数)
(2)Cl:35.5 Cu:63.5
注意:要根据试题中的提供的相对原子质量进行计算或分析。
【例题解析】
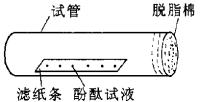
(1)用仪器A吸取浓氨水,滴在脱脂棉上(10~15滴)。A的名称是________,其用途是________。
(2)实验中,观察到的现象是_________,这说明了_________。
(3)实验中,往往在试管下放一张白纸,白纸的作用是_________。
(4)某同学做此实验时,发现滤纸条上没有变色,而试管中所塞的脱脂棉却变成了红色。导致这种现象产生的错误操作可能是_________,这一实验还说明,两种试剂中_________具有挥发性。
【分析】本题主要考察 ①实验的迁移能力,由课本中的演示实验迁移到此实验,原理均相同:酚酞溶液中滴加浓氨水,溶液变红。酚酞与浓氨水分开,由于浓氨水易挥发,分子在不断运动,运动到有酚酞的滤纸条上,使得滤纸条变红。②实验观察能力:靠近脱脂棉的滤纸条部分先变红。③基本实验仪器的名称及其用途
【答案】
(1)胶头滴管 取少量液体
(2)滤纸条从右往左逐渐变红 氨分子在不断的运动
(3)对照,便于观察滤纸条的颜色变化
(4)浓氨水滴在滤纸条上,而酚酞滴在脱脂棉上 浓氨水
A.它的一个分子内含有60个碳原子 B.它是一种新型的化台物
C.它是一种单质 D.保持该物质化学性质的最小粒子是C60分子
【分析】本题主要考查学生的知识迁移能力。C60,其中“60”表示一个C60分子中含有60个碳原子。由于是由一种元素组成的纯净物,故而是单质,不是化合物。由分子构成的物质保持其化学性质的最小微粒就是分子。所以本题选B。

【分析】 分子是保持物质化学性质的最小粒子。所以水的化学性质是由水分子来保持的。选项A表示的是氧原子,选项B表示的是氢原子,选项C表示的是水分子,每个水分子由两个氢原子和一个氧原子构成,它是保持水的化学性质的最小粒子,选项D表示的是氢分子,每个氢分子由两个氢原子构成,它是保持氢气化学性质的最小粒子。所以本题应选C。
 不包含关系,若最大的圆圈代表纯净物,下列选项正确的是
不包含关系,若最大的圆圈代表纯净物,下列选项正确的是A.①单质、③氧化物 B.②化合物、④氧化物
C.①单质、③化合物 D.②含氧化合物、④氧化物
【分析】本题主要考察概念的理解。理解概念才能理清概念之间的关系。
由一种物质组成的是纯净物,纯净物分两类,单质(由一种元素组成的纯净物)和
化合物(由两种或者两种以上元素组成的纯净物)。化合物中如果含有氧元素,则称
为含氧化合物,若只有两种元素组成的化合物,其中一种元素是氧,则称为氧化物。所以氧化物包含于含氧化合物中。所以①是单质②是化合物③含氧化合物④氧化物
【答案】B
