| 中文域名: 古今中外.com
英文域名:www.1-123.com 丰富实用的教育教学资料 |
| |
| |
| |
|
|
11.某同学观察了如右图所示的实验后,得出以下结论,你认为其中不合理的是( )
 A.氯化氢分子和氨分子是不断运动的 A.氯化氢分子和氨分子是不断运动的
B.氯化氢和氨气能发生化学反应
D.两瓶无色气体混合后瓶内压强增大 12.有些游泳池中的水呈蓝色,是因为加入了一种能杀菌消毒的物质。这种物质可能是( ) A.明矾 B.食盐 C.硫酸铜 D.熟石灰 13.纳米材料在军事上有广泛用途,美国军用飞机F-117的表面就涂有隐身材料――纳米氧化铝等。氧化铝的化学式书写正确的是( ) A. AlO B.AL2O3 C.Al2O3 D.Al3O2 14.国外医学界研究表明,假如人体不缺乏微量元素而随意过量补充,不仅对健康无益,反而有害。下列元素属于人体中微量元素的是( ) A.碳 B.氢 C.氧 D.碘 15.下列有关物质的检验或区分方法中不正确的是( ) A. 向某物质中加入稀盐酸,有无色气体放出,则证实该物质是碳酸盐 B. 鉴别氧气和空气两瓶气体时, 将燃着的木条分别插入瓶中,燃烧更旺的为氧气 C. 鉴别铁粉和石墨粉时,分别加入稀盐酸,若有气体放出,则证实为铁粉 D.某化肥与碱共热,若产生使湿润红色石蕊试纸变蓝的气体,证实为铵态氮肥 二、填空与简答题 16.化学就在我们身边,它能改善我们的生活。请从“A.氧气 B.氮气 C.生石灰 D.熟石灰 E.食醋 F.尿素 G.不锈钢 H.聚乙烯”中选择适当的物质填空(填字母)。 (1)抢救危重病人常用的物质是 ;(2)用于农作物肥料的物质是 ; (3)常用作袋装食品干燥剂的是 ;(4)厨房调味品中pH小于7的是 ; (5)可以制成食品包装袋的是 ;(6)可用于制造刀具的物质是 ;
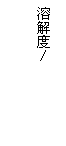  17.溶解度曲线为我们定量描述物质的溶解性强弱提供了便利。请你根据右图的溶解度曲线回答下列问题: 17.溶解度曲线为我们定量描述物质的溶解性强弱提供了便利。请你根据右图的溶解度曲线回答下列问题:
(1)20℃时,甲物质的溶解度_____ (填“大于”、“等于”或“小于”)乙物质的溶解度。 (2)_______ ℃时,两种物质的溶解度相等。 (3)60℃时,将80 g 甲物质放入100 g水中,所得溶液的溶质质量分数为 。 18.趣味化学联欢会上,小刚和小强给同学们变起了“魔术”、小刚说:“我会‘水变汽水”。 他边说边将两种无色澄清的液体倒在一起,马上得到一杯冒着气泡的澄清液体。小强说:“这没什么,我还会‘水变牛奶’呢”。只见他将两种无色澄清的液体倒在一起,果真得到一杯像是‘牛奶’的液体。 (1)“水变汽水”所用的两种澄清液体可能是_________________________________。 (2)“水变牛奶”的“魔术’可以通过许多化学反应来完成,例如(用化学方程式表示)_______________________________________________________________。 (3)请你再设计一个化学“魔术”,写出“魔术 名称和化学反应原理。 ________________________________________________________________。 19. 今年冬天我国内蒙古发生了多起CO中毒事故。由此引发了同学间的争论:
请说出你的看法及理由: 。
| 液体
| 血液
| 胰液
| 胃液
| 胆汁
| pH范围
| 7.35~7.45
| 7.5~8
| 0.9~1.5
| 7.1~7.3 |
请回答:液体碱性最强的是 。
|
|
一种治疗胃病药物的标签。请回答:
该药物在胃中发生的化学反应的化学方程式是 。
21.
|
饱和硝酸 钾溶液 |
|
浓硫酸 |
 小强设计了一个有趣的实验(如右图所示),经过很长一段时间后,他观察到小试管内有晶体析出。
小强设计了一个有趣的实验(如右图所示),经过很长一段时间后,他观察到小试管内有晶体析出。
(1)下面是小强对这种现象解释的部分内容,请你帮他把其余的解释内容续写完整:浓硫酸具有吸水性,
。
(2)若实验前后温度不变,则实验后的硝酸钾溶液的溶质质量分数 (填“大于”、“等于”或“小于”)原饱和硝酸钾溶液的溶质质量分数。
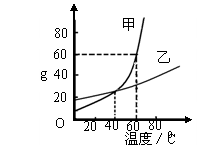
22.“探险队员”~盐酸,不小心走进了化学迷宫(下图所示),不知怎样走出来,因为迷宫中有许多“吃人的野兽”(即能与盐酸发生反应的物质),盐酸必须避开它,否则就无法通过。请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线)。
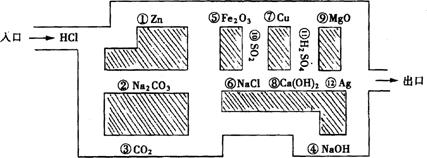
入口→ → → → → → →出口。
23.化学是造福人类的科学,在人体保健、医疗卫生等方面作出了重大贡献。请你用所学的化学知识解答有关问题。
(1)食品安全与健康密切相关。下列做法不会危及人体健康的是( )。
A. 用“苏丹红一号”作食品添加剂 B .蒸馒头时加入适量纯碱
C.加过量亚硝酸钠以保持肉质鲜美, D.把霉大米淘净后继续食用
(2)低血糖患者天天都应注重摄入一定量含淀粉的食物,以使血液中维持一定浓度的葡萄糖。请你列举两种富含淀粉的食物 、 。
(3)油炸食物不宜多吃,因长时间煎炸会产生有毒物质丙烯醛(C3H4O),丙烯醛在空气中完全燃烧时,生成二氧化碳和水。请写出丙烯醛完全燃烧的化学方程式 。
(4)食盐是人维持正常生理活动的重要物质。人体细胞中约含NaCl 0.9%,一般成年人每日需NaCl的量为4.5 g~9 g。
①某病人因食盐摄入量不足,需要补充溶质质量分数约为0.9%的生理盐水,现医生确定天天为他注射200 g生理盐水,则天天可为他补充约 g食盐。
②小明同学根据NaCl AgNO3=AgCl↓(白) NaNO3这一反应原理,对一瓶生理盐水进行分析时,不知道加入的硝酸银溶液与氯化钠溶液是否恰好完全反应,于是他设计了一个实验方案进行探究。请你帮他完善该实验方案。
探究步骤
可能观察到的现象
结论
(1)取反应后的上层清液于试管中,滴加 溶液
若有白色沉淀生成
溶液过量
若无白色沉淀生成
还需进行下一步探究
(2) 另取反应后的上层清液于试管中,滴加 溶液
三、实验与探究题
24.为了研究CO2的性质,需要制取并收集干燥的CO2气体。以下是老师提供的一些实验装置。
|
稀HCl |
|
NaOH溶液 |
|
浓H2SO4 |
|
CaCO3 |
|
A |
|
B |
|
C |
|
D |
|
E |
|
F |
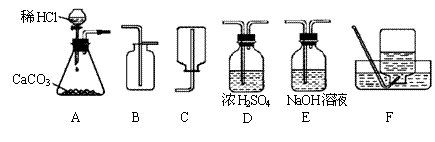 |
(2)实验室制取CO2的化学方程式为 。
(3)若在上述实验中气体无法收集满,则可能的原因是 。
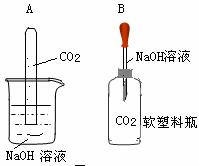 25.化学反应往往伴随着一些现象的发生,但CO2与NaOH溶液的反应没有明显的现象。为了通过一些现象说明CO2与NaOH溶液发生反应,小明和小华分别设计如图两个实验进行探究。
25.化学反应往往伴随着一些现象的发生,但CO2与NaOH溶液的反应没有明显的现象。为了通过一些现象说明CO2与NaOH溶液发生反应,小明和小华分别设计如图两个实验进行探究。
观察到A装置中试管液面上升。B装置的现象为 。同学们经过分析讨论,A 实验中产生液面上升的原因可能有两种。一种是因为CO2与NaOH溶液发生反应,消耗CO2,你认为另一种原因是 。
为了进一步证实CO2与NaOH溶液反应。你认为小华同学应该补做的实验是
。
26.聪聪在用水煮虾的过程中发现青色的生虾煮熟以后变成红色,非凡是虾汤的颜色更是鲜红。
(1)提出问题:虾汤中的这些红色物质是什么?
(2)猜想与假设:这种红色物质可能像酸碱指示剂一样,遇酸或遇碱,颜色会发生改变。
(3)收集证据:现在请设计一个简单的探究方案,验证聪聪的猜想:
使用的试剂
实验操作方法
可能的现象
(4)以上的探究对你有什么启示?
。
四、计算与分析题
27.一题多解能启迪同学们的思维。如:电解18g的水最多能产生多少克氢气?晓梦同学认为可以根据化学方程式计算。小莹同学认为只要求出18g水中所含氢元素质量便可知道反应生成的氢气质量。小莹同学的解题依据是 。
请你用小莹同学的解题方法把解题过程写出来。
28.散装过氧化氢溶液溶质质量分数约为30% 。小明同学用它来配制溶质质量分数为5%的过氧化氢溶液,做如下实验:取该溶液10g放入烧杯中并加入90g的水,搅拌,再加入1g MnO2 充分反应,质量不再减轻后,称得剩余物及烧杯总质量为171.8g。(烧杯质量72.1g)
求: = 1 \* GB3 ①反应生成的氧气质量为多少?(精确到0.1g)
= 2 \* GB3 ②原溶液溶质质量分数为多少?(精确到0.1%)
= 3 \* GB3 ③配制200g 质量分数为5%的过氧化氢溶液,需要该桶装溶液多少克?(精确到0.1g)
化学反应方程式:2H2O2 ![]() 2H2O O2↑
2H2O O2↑
参考答案
一、选择题
题号
1
2
3
4
5
6
7
8
9
答案
C
A
D
B
B
A
A
B
C
题号
10
11
12
13
14
15
答案
A
D
C
C
D
A
二、填空与简答题
16.(1)A (2)F (3)C (4)E (5)H (6)G
17.(1)小于 (2)40 (3)37.5%
18. (1)碳酸钠溶液(碳酸氢钠溶液)、稀盐酸(或其他稀酸)
(2)Na2CO3 Ca(OH)2=== CaCO3↓ 2NaOH
(3)“白酒变红酒”酚酞试液遇碱变红(或表述为:将滴有酚酞试液的水和氢氧化钠溶液混合得到红色溶液)
19.都不完全正确,CO虽然对环境会造成污染,但合理利用可以为人类生产、生活服务。
(言之无理或提出错误观点不能给分)
20.胰液 Al(OH)3 3HCl === AlCl3 3H2O
21.(1) 浓硫酸具有吸水性,可以吸收硝酸钾溶液中挥发出的水分,使饱和溶液中的溶剂减少,溶质析出。(2)等于
22.入口→③→⑥→⑩→⑦→11→12→出口
23.(1)B (2)略 (3)2C3H4O 7O2 === 6CO2 4H2O (4) ① 1.8
②合理答案均可。
探究步骤
可能观察到的现象
结论
(1) NaCl
AgNO3
(2))AgNO3
若有白色沉淀生成
NaCl
若无白色沉淀生成
两者恰好完全反应
三、实验与探究题
24.(1)A、D、C (2)略 (3)药品量不足或气密性不好等。
25.软塑料瓶变瘪 CO2与NaOH溶液中的H2O发生反应(或CO2溶于 NaOH溶液中的H2O),消耗CO2
26.稀盐酸、 NaOH溶液 把红色的虾汤分成三份;向一份中加入稀盐酸,向另一份中加入NaOH溶液与第三份进行颜色对比 加入酸或碱的虾汤的颜色可能会发生变化
(4)要像聪聪那样,善于观察、善于发现、善于思考、大胆猜想;对比实验是一种重要的科学方法。
四、计算与分析题
![]() 27.质量守恒定律
27.质量守恒定律
18g水中所含氢元素质量=
根据质量守恒定律反应生成的氢气质量为2g。
28. = 1 \* GB3 ①1.3g
= 2 \* GB3 ②设:10g样品中所含H2O2 质量为x。
2H2O2 ![]() 2H2O O2↑
2H2O O2↑
68 32
X 1.3g 1分
![]()
X=2.76g 1分
![]()
该样品H2O2溶质质量分数=
答:(略)
= 3 \* GB3 ③设:需该桶装溶液质量为y。
y×27.6%==200g×5% 1分
y=36.2g 1分
答:(略)
| |