一、选择题(本题包括14小题,每小题2分,共28分。每小题有1个或2个选项符合题意。若有两个答案的错1个不得分,漏选1个扣1分。)1、种植下面几种农作物对pH的要求是:大豆6~7,茶5~5.5,甜菜7~7.5,西瓜6。如果某地区经常降酸雨,则?D上述农作物最不适合种植的是( )。
A、大豆 B、茶 C、甜菜 D、西瓜
2、一种“即食即热型快餐”适合外出旅行时使用。其内层是用铝箔包裹的、并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是( )。
A、浓硫酸与水 B、生石灰与水 C、熟石灰与水 D、氯化钠与水
根据以下提供的材料,解答第3~5题。
材料1:据2002年4月30日《中国环境报》报道,某化工厂排放的污水,使某市一条长约50 km的河水受到严重污染,对工农业生产及人民的生活造成严重危害。经环保部门测定,被污染的河水pH在1~4之间,其他水质指标也严重超标。
材料2:2002年6月1日,国家环境保护总局发布的《地表水环境质量标准》,对地表水质量作了明确规定,部分指标如下(除pH外,各项目的单位:mg/L):
|
项目及标准 |
水质分类 | ||||
|
I类 |
Ⅱ类 |
Ⅲ 类 |
Ⅳ类 |
Ⅴ类 | |
|
磷(P)≤ |
0.02 |
0.1 |
0.2 |
0.3 |
0.4 |
|
氮(N)≤ |
0.2 |
0.5 |
1.0 |
1.5 |
2.0 |
|
锌(Zn)≤ |
0.05 |
1.0 |
1.0 |
2.0 |
2.0 |
|
铅(Pb)≤ |
0.0l |
0.01 |
0.05 |
0.05 |
0.1 |
|
pH |
6~9 |
6~9 |
6~9 |
6~9 |
6~9 |
3、如果让你测定该河水样的酸碱度,可选用( )。
A、石蕊试液 B、酚酞试液 C、pH试纸 D、碳酸钠溶液
4.材料2中所指出的“氮”、“磷”、“锌”、“铅”,是指( )。
A、单质 3、元素 C、离子 D、分子
5、经测定,该化工厂排放的污水中铅的质量分数为(1×10-5)%。则该污水的水质属于(设该污水的密度为1g/cm3)( )。
A、Ⅰ类 B、Ⅲ类 C、Ⅳ类 D、V类
6、我国科学家在1993年首次利用超真空扫描隧道显微镜技术,在一块晶体硅(由硅原子构成)的表面直接移动硅原子写下了“中国”两字(见图)。下列说法中正确的是( )。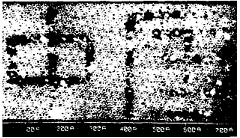
A、在上述操作中没有任何变化
B、这两个汉字是当时世界上最小的汉字
C、此技术说明在化学变化中原子可以再分
D、标志着我国科学家已进入了操纵原子的阶段
7、据报道,某地发现?D温泉,水温高达58℃。经监测分析,该温泉属硅酸盐矿泉,有软化血管的作用,对心脏病、高血压病等有良好的医疗保健作用。已知硅酸盐中硅元素的化合价为+4价,则硅酸的化学式为( )。
A、H2SO4 B、H4SiO3 C、 H2SiO3 D、Na2SiO3
8、某工厂排放的废硫酸,拟选用下列物质与之中和。如果要求花最少的钱来中和同样量的废硫酸,则应选择( )。
|
|
物质 |
相对分子质量 |
市场参考价(元/kg) |
|
A、 |
CaCO3 |
100 |
1.8 |
|
B、 |
Ca(OH)2 |
74 |
2.0 |
|
C、 |
NH3 |
17 |
6.5 |
|
D、 |
NaOH |
40 |
11.5 |
9、燃料电池是一种将化学反应产生的能量直接转换成电能的装置。下列燃料电池比较适合宇宙飞船上使用的是( )。
A、CH4?DO2燃料电池 B、C2H5OH?DO2燃料电池 C、H2?DO2燃料电池 D、CO?DO2燃料电池
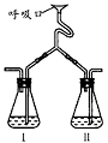 10、为验证人体呼出气体中含有的CO2不是来自空气,而是人体代谢作用产生的。某学校学生课外活动小组设计了如右图所示装置,你认为该装置应选用的试剂是( )。
10、为验证人体呼出气体中含有的CO2不是来自空气,而是人体代谢作用产生的。某学校学生课外活动小组设计了如右图所示装置,你认为该装置应选用的试剂是( )。
瓶I 瓶Ⅱ
A、 Ca(OH)2 NaOH
B、 NaOH Ca(OH)2
C、 稀HCl Ca(OH)2
D、 NaOH BaCl2
11、甲原子与乙原子的质量比为a∶b,而乙原子与碳12原子的质量比为c∶d,则甲原子的相对原子质量为( )。
A、12ac/bd B、bc/12ac C、12bd/ac D、ab/12bc
12、将wgKNO3的不饱和溶液恒温蒸发水分,直到有晶体析出。在此变化过程中,溶液中溶质质量分数与蒸发时间的变化关系可用下图表示的是( )。
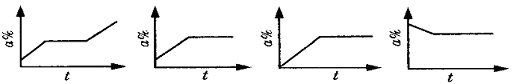
A B C D
13、为了使经济可持续发展,生产过程应尽量减少对环境的负面作用。由单质铜制取硫酸铜有下列几种步骤,其中可行且符合以上要求的是( )。
A、Cu→CuSO4 B、Cu→CuO→CuSO4
C、Cu→Cu2(OH)2CO3→CuSO4 D、Cu→Cu(NO3)2→Cu(OH)2→CuSO4
14、50g镁、锌、铁的混合物与足量的稀硫酸反应得到混合溶液,蒸发后得到218g固体(已换算成无水硫酸盐)。则反应产生氢气的质量是( )。
A、2 g B、3 g C、3.5g D、4.5 g
二、填空题(本题包括9个小题,共41分)
15、(6分)反物质是由反粒子组成的物质。所有的粒子都有相应的反粒子,反粒子的特点是其质量、寿命等与相应的粒子相同,但电荷、磁矩等与之相反。反粒子一旦与相应的粒子碰撞,如电子碰到反电子,就会立即“湮灭”为其他物质。据最新报导,欧洲核子研究中心近日成功地制造出约555个低能量状态的反氢原子,这是人类首次在受控条件下大量制造的反物质。试回答下列问题:
(1)你认为反氢原子的结构示意图可表示为 ,图中代表各微粒的符号及其所表示的意义分别是:
表示 ; 表示 。
(2)质子与反质子相碰撞而“湮灭”是化学变化吗? ,理由是 。
16、(2分)用来制蜡烛的石蜡是一类含碳、氢元素的化合物,可用通式CnH2n+2表示其组成。在空气中点燃蜡烛,常因燃烧不完全而产生炭。室内有人吸烟后,常有难闻气味,有人建议,在室内点燃一支蜡烛,不久这种气味可减弱,其原因是 。
17、(3分)吸烟有害健康,科学实验表明香烟所产生的烟雾中,至少有300多种化合物不同程度对人体有害。为了检验该烟雾中是否存在CO2和CO,在对香烟燃烧产生的烟雾进行适当处理后,依次通过足量的以下试剂:①澄清石灰水,②浓硫酸,③灼热的黑色氧化铜粉末,④澄清石灰水,发现①④变浑浊。试回答:
(1)①中发生的现象说明 。
(2)烟雾中是否存在CO? ,做出此判断依据的实验现象为 。
18、(3分)人们每天通过摄取食物不断补充所需要的各种元素,但有时也会摄入某些有害的元素。请指出下列矿物元素中,哪些是人体必需的微量元素,哪些是对人体有害的微量元素(请用线连接)。
镉Cd
铜Cu
铁Fe
钙Ca
汞Hg
必需的微量元素 碘I 有害的微量元素
铅Pb
镁Mg
硒Se
锌Zn
19、(5分)实验室现有五瓶失去标签的无色溶液,根据实验室的记录,只知它们分别是KCl、K2SO4、K2CO3、AgNO3、BaCl2中的一种,为确定它们的成分,某学生将它们依次编为A、B、C、D、E,并设计了一组实验。实验记录如下:
(1)将A和B混合,产生一种既不溶于盐酸也不溶于稀硝酸的沉淀;
(2)将C和D混合,产生一种既不溶于盐酸也不溶于稀硝酸的沉淀;
(3)将A和E混合,产生的沉淀既溶于盐酸也溶于稀硝酸;
(4)将D和E混合,产生的沉淀仅在稀硝酸中消失;
(5)将B和C混合,没有沉淀生成。
由以上实验确定:A是 ,B是 ,C是 ,D是 ,E是 。
20、(3分)实验室用锌粒和稀硫酸反应制取氢气,并经过净化、干燥后,还原氧化铜来测定铜的相对原子质量。根据所得到的铜粉的质量,可求得参加反应的氢气的质量,进而计算出应消耗的锌粒和稀硫酸的质量。但实际耗用的锌粒(不含杂质)和稀硫酸的质量都远远超过计算值。试从实验过程看,原因是 。
21、(4分)新型材料纳米级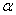 -Fe。请回答以下问题:
-Fe。请回答以下问题:
(1)写出生成纳米
(2)反应中保护气的作用是 。
请回答以下问题: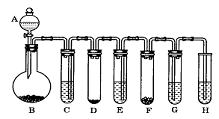
(1)实验开始前必须进行的操作是 ;
(2)反应开始后,若G中出现红色,H中有白色沉淀生成,判断E、F中的物质可能分别是 , ;
(3)按基本反应类型写出该实验中有关反应的化学方程式(装置用字母表示):
化合反应 ,发生在装置 中;
分解反应 ,发生在装置 中;
置换反应 ,发生在装置 中;
复分解反应 ,发生在装置 中。
23.(4分)测定人体血液循环量的一种方法是:吸取6.0mL含放射性元素131I?D人血清白蛋白溶液,每1.0mL含放射性元素碘2.0×10-6Ci(居里,一种放射性强度的单位),快速注入静脉中,10min时抽取1.0mL静脉血液,测定其中含放射性元素碘为0.003 0×10-6Gi(10 min内碘的放射性的强度改变可忽略不计)。人的血液循环量为 L。
又知碘是甲状腺素的主要成分,健康成人每天适宜摄入量为100μg~200μg(1μg为1×10-6g)。为使上述测定结果可靠,从测定人体血液循环量24 h前,连续5d服用碘化钠(不含放射性碘)50mg/(5mL?d),原因是 。
三、实验题(本题包括3小题,共18分)
24、(5分)某生活污水有一股臭味,主要含有碎菜叶、碎塑料薄膜、泥沙、氯化钠和碳酸钠等物质。现欲将其经去渣、除臭处理后用于清洗厕所的用水。问:
(1)采取何种操作可除去其中的固体物质 ;
(2)用什么物质可除去污水的臭味 ;
(3)把生活污水进行处理再利用的目的是什么 ;
(4)怎样检验经(1)和(2)处理后的水中是否还存在氯离子 。
25、(7分)将适量黄色的草酸亚铁(FeC2O4?2H2O)粉末加入试管,在酒精灯上边加热边摇动,发生剧烈反应,产生的气体可使燃着的木条熄灭,生成黑色的粉末。反应将结束时,用橡皮塞塞好试管,稍冷后,打开塞子将所得的黑色粉末撒在石棉网上,便会立即自燃起来。试回答下列问题:
(1)黑色粉末是什么物质?为什么在空气中自燃? ;
(2)反应将结束时,用橡皮塞塞好试管有何作用? ;
(3)化学反应的快慢与反应物的表面积有何关系? ;
26、(6分)雷利是英国物理学家,他曾用下列两种方法测定氮气的密度。
方法一:将除去水蒸气和二氧化碳的空气通过烧红的装有铜屑的玻璃管,使空气中的氧气全部除去,测得氮气的密度为1.2572g/L。
方法二:将氨气(NH3)通过赤热的装有氧化铜的玻璃管,生成氮气和水蒸气,除去水蒸气后测得氮气的密度为1.2508g/L。若两次测定时的状况相同,请问:
(1)方法二中发生反应的化学方程式为 ;
(2)欲除去空气中的水蒸气和二氧化碳,可供选择的装置如图所示(不可重复使用),在你选择的装置中,用相应的字母表示导管口的连接顺序 ,瓶中应盛放什么物质 。
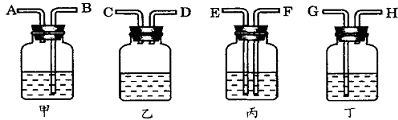
(3)请分析两种方法所测定的氮气密度数值不同的原因。 。
四、计算题(本题包括2小题,共13分)
27、(7分)现有一种铜和氧化亚铁的混合物样品。为测定该样品中氧化亚铁的含量,某学生取20.0g此样品置于烧杯中,分四次加入密度为1.22g/cm3的硫酸并做相关记录。有关数据记录如下:
加硫酸的序号 加入硫酸的体积/mL 剩余固体的质量/g
1 20.0 16.0
2 20.0 12.0
3 20..0 8.0
4 20.0 8.0
试计算:
(1)10.0g此样品中铜的质量。
(2)样品中氧化亚铁的质量分数。
(3)所用硫酸溶液溶质的质量分数。
28、(6分)航天技术中的火箭推进剂可用醇类为燃料,液态氧为氧化剂,但后者的沸点较低(-183℃),需要额外的隔热装置,因而增加了火箭的重量。为了避免此缺点,可用过氧化氢(H2O2)代替液态氧,它具有相对高的沸点和较低的凝固点,而且没有毒性,和醇反应时也能放出很高的能量。现有一液体推进剂以醇(含碳52%、含氢13%、含氧35%)为燃料,质量分数为90%的过氧化氢做氧化剂,欲使1 kg该醇燃料完全燃烧,计算需消耗质量分数为90%的过氧化氢的质量。(可按2H2O2→2H2O↑+O2↑得到的氧气与醇反应来计算
参考答案2003年全国初中学生化学素质和实验能力竞赛(第十三届天原杯)复赛试题
一、选择题
1.C 2.B 3.C 4.B 5.D 6.B、D 7.C 8.B 9.C 10.A 11.A 12.B、C 13.B 14.C
二、填空题
(1)
(2)不是。 化学变化是反应物中原子的重新组合,“湮灭”不是
17、(1)燃烧产物中存在CO2 (2)存在 ④中的澄清石灰水变浑浊
18、
19、BaCl2,K2S04,KCl,AgNO3,K2CO3
20、①氧化铜加热前要先通氢气,排去试管内空气;②反应后热铜粉还需在氢气中冷却;③部分氢气通过装有氧化铜的试管时,未与氧化铜反应
21、(1)H2+FeCl2高温Fe+2HCI (2)防止生成的纳米Fe被氧化
22、(1)检查装置的气密性(2)稀盐酸,石灰石(其他合理答案也可得分)(3)化合反应 CO2 + H2O =H2CO3 G 分解反应 2H2O22H2O + O2↑ D 置换反应 Zn十H2SO4=ZnSO4 + H2↑ B复分解反应 CaCO3 + 2HCI=CaCl2 + H2CO3 F
23、4.0 L 减少注入的放射性元素碘被甲状腺吸收。
三、实验题
24.(1)沉降,过滤 (2)活性炭,木炭,吸附剂,除臭剂,微生物作用(答对一种即可)
(3)节约用水 (4)取2mL待测液于试管中,滴加硝酸银溶液,若有白色沉淀生成,加稀硝酸酸化,若白色沉淀不消失,则证明待测液存在氯离子
25、(1)铁粉。由于生成的铁粉很细,极易氧化并产生热量使铁粉达到着火点引起自燃
(2)防止铁粉被氧化 (3)反应物表面积越大,反应越快
(4)FeC2O4·2H2O
26、(1)2NH3 + 3CuO
(2)BAGH或GHBA
上述装置顺序中,第一个盛放氢氧化钠溶液,第个盛放浓硫酸
(3)空气中含有少量密度比氮气大的气体,使得方法一的测定值偏高
四、计算题
27、(1)4.0g (2)60.0% (3)22.3%
28、4904 g
