一、选择题。在下列各题的四个选项中,只有一个选项是最符合题目要求的(共30分)
1.化学使世界变得更加绚丽多彩,化学变化在我们周围到处存在。下列属于化学变化的是
A. 冰雪融化 B. 海水晒盐 C.汽油挥发 D.铁锅生锈
2.乐山大佛───峨眉山是世界文化和自然遗产。打造“中国第一山”已成为乐山人的共识。从优化环境,防止污染
的角度看,下列作法中,你认为错误的是
A. 景区车辆使用电动车 B.将景区内住户搬迁,减少生活垃圾污染
C.将生活垃圾就地焚烧 D.强化生活垃圾的分类回收 、
3.下列物质在水中不能形成溶液的是
A. 奶粉 B.高锰酸钾 C.酒精 D.蔗糖,
4.下列有关物质性质的利用叙述中错误的是
A. 甲醛具有破坏蛋白质结构的性质,所以可以用甲醛溶液浸泡食用海产品以杀菌
B.用肥皂水区分硬水与软水是利用了硬水遇肥皂水会起浮渣的性质
C.装食品的聚乙烯塑料袋用加热方式封口,是因为该塑料具有热塑性
D.碳酸氢钠用于焙制糕点是利用了它能反应生成C02气体的性质
5.下图是氧化汞分解生成汞和氧气的分解示意图。根据图示的推理中,正确的是

① 物质发生化学反应是分子的破裂,原子的重新组合
② 分子是保持物质化学性质的最小粒子
③ 原子是化学变化中的最小粒子
④ 化学变化中的质量守恒是因为反应前后原子种类和数目没有变化
A. ①② B.③④ C. ②③④ D.①②③④
6. 水是人类不可缺少的物质,水可以造福人类;但水污染后给人类造成灾难。在化学研究中,水既可以作反应物,也可
作生成物,同时水也是最常用的溶剂。下列叙述的有关 判断中,错误的是
A. 成年人体内含约70%的水───水是构成人体的物质
B.化工厂排出的已污染的废水───—水是溶剂
C.甲烷在空气中燃烧产生水───—水是生成物 .
D.二氧化碳溶于水后生成碳酸───—水是生成物
7.下列各组中的化学方程式与所述事实不符合的是
A. 氢气是最清洁的燃料 :2H2+O2![]() 2H2O
2H2O
B.葡萄糖在酶作用下被氧化:C6 H12O6+6O2![]() 6CO2+6H2O
6CO2+6H2O
C.用稀硫酸洗去试管壁上附着的铜:Cu+H2SO4 = CuSO4+H2 ↑
D.用盐酸除铁锈:Fe2O3+6HCl = 2FeCl3+3H2O
8.下列试剂中,不能将酚酞和碳酸钠两瓶无色溶液鉴别开的是
A. NaOH B.NaCl C. 盐酸 D.Ca(OH)2
9.逻辑推理是化学学习中常用的方法,下列推理中错误的是
A. 自来水的消毒剂C1O2中,C1元素的化合价是+4价
B.某物质在空气中燃烧生成水和二氧化碳,该物质一定由碳、氢、氧三种元素组成
C. 某物质在氧气中燃烧产生蓝紫色火焰,该物质可能是硫
D.碳在空气中燃烧不如在氧气中燃烧旺;镁与酸反应比锌与酸反应强烈;这两个例子说明反应物的量和反应物的性质影
响反应剧烈程度
10.下例图像与事实不符的是
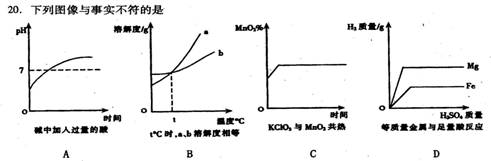
11. 物质的组成—结构一性质一变化有着密切的关系,这种关系是化学知识的基本结构。下列关于反应
![]()
(注:0、+3、—2表示元素化合价)所进行的判断推理中,正确的是
①氧气使铝发生氧化反应,故氧气具有氧化性
②反应中,铝元素的化合价由0价变为+3价,氧元素的化合价则降低为—2价。
③氧气具有氧化性是因为氧原子最外层电子数为6,在化学反应中易得电子,元素化合 价降低
④金属铝原子在化学反应中失去电子,被氧化,其元素化合价升高,故铝具有还原性
A.①② B.③④ C.②③④ D.①②③④
12.将一定量的碳和氧气放人一密闭容器中燃烧,待氧气耗尽时得到20g气体,将该气体通过足量的石灰水后,气体剩余
11.2g,则反应前密闭的容器中氧气的质量克数是
A. 16g B. 13.2g C.6.4g D. 12.8g
三、填空题(本大题包括7个小题,共25分) .
13. (4分)日常生活你会遇到许许多多的物质,首先你要知道它的成分。请用化学符号表示:
(1)地壳中含量最多的金属元素 ;
(2)防毒面具用来作吸附剂的物质是 ;
(3)天然气中的“气’’是 ;
(4)由三个氧原子构成的臭氧分子 。
14.(5分.)我市许多区、县的地下贮藏着大量的碳酸钙,由碳酸钙构成的地貌特点是溶洞、钟乳石等奇观多,其原因是
当遇到溶有二氧化碳的水时,碳酸钙会反应生成可溶性碳酸氢钙[CaCO3+CO2+H2O=Ca(HCO3)2:]而溶于水中。碳酸氢钙在一
定条件又分解生成碳酸钙而沉积形成不同奇观。请回答问题:
(1) 这些区、县的天然水中一定含较多的 ;这种水属于 (选填硬水、软水),用水壶烧这种水会形成 ;
(2) 这些区、县的工业生产中,石灰厂、水泥厂较多,原因是 ;
有些地方还盛产建筑、装饰用的材料,俗名叫 ,它与钟乳石的化学成分相同。
15.(3分) 关于粒子 ![]()
属于何种粒子,请你作出判断:
(1) ①例:如果n小于10,则该粒子是阴离子;
② ;
③ ;
(2) 如果该粒子所表示元素的原子的质子数是11,请写出该元素原子的结构示意图 。
16.(5分) 对比、分析是学习化学的一种重要方法。现有反应①Fe+2HCl=FeCl2+H2↑;
②Fe+CuSO4=FeSO4+Cu;③ Cl2+2KBr=2KCI+Br2;④Br2+2KI=2KBr+I2
(1) 通过比较分析可以发现,它们的相似之处是都属于 反应。请你写出一个符合这个条件的化学反应方程式 。
(2) 从第①个反应中可得到的信息是 ;
从第②个反应中可推出Cu和Fe的化学活动性强弱顺序是 ;
(3) 通过第②个反应的推论,再迁移到第③④个反应中,可得出I2、Br2、Cl2三种单质的非金属活动性强弱顺序为 。 .
17.(3分) 已知A、B、C是常见的酸和碱,它们能相互发生如下反应:A+B=NaCl+H2O
C+BaCl2=BaSO4↓+A,试判断A、B、C各为何种物质。并填空:
(1) 写出A的化学式 ;
(2) 写出B物质的一种化学性质 ;
(3) 写出有C物质参加的复分解反应 。
18.(3分) 植物生长需要氮,氯化铵[NH4Cl]是一种常用的氮肥。计算并回答:
(1) 氯化铵中各元素的质量比为 ,氯化铵中氮元素的质量分数是 ;
(2) 氯化铵不能跟熟石灰混用的原因 。
19.(2分) ①据报道,某地制钠(Na)厂发生了一起氯气(C12)泄漏事故。请你根据所学的知识和这一信息猜想,该制钠
厂生产需要购进的一种原料。该原料的名称是 。
② 某同学在兴趣小组活动时,将MnO2,、CaO、Mg(NO3)2三种物质与H2O2溶液混合。
请你帮助他分析推断,该物质混合后可能发生的化学反应有 个。
四、实验题(本大题包括2个小题,共10分)
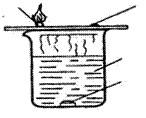
20.(4分) 下图是可燃物燃烧条件的探究实验。根据科学探究方法,它们分别为两组对照实验,a、c为一组,a是研究
实验,c为对照实验。这一组的变量是可燃物的着火点不同,实验说明可燃物的 是燃烧条件之一,即温度是否达到
可燃物的着火点。
在a、b这组实验中, 是对照实验,变量是 ,此时a着火燃烧而b不燃烧,说明氧气是可燃物燃烧的条件之一。
要使b处白磷发生燃烧,在本实验中可采用的方法是
21.(4分) 草酸(H2C2O4)是一种无色固体,实验室用来加热制取CO气体,反应方程式为
H2C2O4![]() CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
(1) 加热草酸制CO气体的发生装置应选用 。(选填:A用高锰酸钾制氧气的装 置;B实验室制二氧化碳装置)
(2) 为探究草酸分解一定生成了CO和CO2,小李同学设计了如下实验。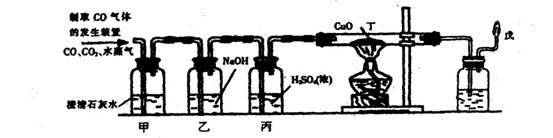
请回答下列问题:
① 甲瓶中可观察到的现象是 ;证明 ;
② 混合气体通过乙瓶和丙瓶,得到的是 ;
③ 丁处出现红色物质的原因是 ;(用化学方程式表示)
④ 戊处进行尾气处理的目的是 。
五、探究与计算(本大题有1个小题,共10分)
22.(10分)科学探究是奇妙的过程。某同学在实验室进行如下探究活动,请你参与,并帮助他完成下列内容:
(1) [提出问题] 某同学在实验室发现一瓶白色粉末,瓶上标签已失去。他将该粉末取 少量放人试管中,滴入稀盐
酸,有气泡产生。为鉴定该气体的成分,他作了如下探究:
(2) [猜想与假设] 该气体可能是CO2
(3) [设计与实验]
|
实验步骤 |
实验现象 |
实验结论 |
|
用一支玻璃棒蘸取少许澄清石灰 水,插入产生气体的试管中 |
玻璃棒上有白色的物质产生 |
方程式 ; 该气体是CO2,由此可判断该白色 粉末是碳酸盐 |
(4) [讨论与反思] ,
已知白色碳酸盐有Na2CO3,、K2CO3,、CaCO3、BaCO3等。他做了分类归纳:
归纳1:该白色粉末是Na2CO3、K2CO3等可溶性物质
归纳2:该白色粉末是CaCO3、BaCO3等不溶性物质
(5) [实验探究]
实验步骤: ① 取白色粉末少许于试管中,再注入适量水,振荡,粉末全部溶解
② 在①中滴人澄清石灰水,溶液中出现白色沉淀。
结论:该粉末是 。
请你思考判断:该同学做的上述实验中,是否有必要做第②步? ,
为什么? 。
(6) [计算分析]
根据上述实验结论,该同学为确定白色粉末为何种碳酸盐,进行了定量探究。他称取白色粉末6.9g,与20g稀盐酸混合,
刚好完全反应。此时称量,溶液质量为24.7g。
求:①反应中产生二氧化碳的质量克数;
②计算确定白色粉末是碳酸钠还是碳酸钾;
③反应前盐酸溶液的质量分数。
理化生试题参考答案及评分意见
一、1.D 2。C 3.A 4.A 5.D 6。D
7.C 8.B 9.B 10.A 11。D 12.D
二、填空
13.(1)Al (2)C (3)CH4 (4)O3, (每空1分) 共4分
14.(1) Ca(HCO3)2 硬水 水垢
(2) 有充足的生产原料 (CaCO3) 大理石 (每空1分) 共5分
15.② n=10 原子
③ n>10 阳离子 其中②③顺序可调 (2) (每空1分)共3分
16.(1) 置换反应Zn+H2SO4=ZnS04+H2↑ (2分)
(2) 铁可置换出酸中的氢 Fe>Cu (2分)
(3) C12>Br2>I2 (1分) 共5分
17.(1) HCI (2) 使酚酞试液变红或HCl+NaOH=NaCl+H2O
(3) BaCI2+H2SO4=BaSO4↓+2HCI (每空1分) 共3分
18.(1) N:H:C1=14:4:35.5; 26.2% (2分)
(2) 产生氨气逸出,损失肥效 (1分) 共3分
19. (1). NaCI (1分)
(2) 3个 (1分) 共2分
四、(本大题10分)
20.着火点 b 氧气 用导管向白磷处通人O2 <每空1分) 共4分
21.(1) A; (2) ① 澄清石灰水变浑浊;证明草酸反应生成CO2
② 较干燥、纯净的CO
③ CO+CuO ![]() Cu +CO2
Cu +CO2
④ 除掉未反应的CO,防止污染空气 (每空1分)共6分
五、(本大题10分)
22.(3) CO2+Ca(OH)2=CaCO3↓+H2O (1分)
(5) 结论:该粉末是Na2CO3或K2CO3;
没有必要,根据已知条件第①步已经证明 (3分)
(6) ①二氧化碳质量:20+6.9-24.7=2.2g (1分)
② 设白色粉末中金属元素为R,其相对原子质量为r,反应前盐酸的质量分数 为x%
R2CO3 + 2HCI = 2RCI + H2O + CO2↑ (1分)
2r+60 2 x36.5 44
6.9 20xx% 2.2 (1分)
![]()
r=39 (1分)
查相对原子量表知该金属为钾,故原物质为K 2CO3 (1分)
③ ![]()
x%=1 8.3% (1分)
答:略
注:其余解法只要方法合理,参照给分
