化 学
一、本卷,27至38题为化学,每小题3分;共36分。在下列各题的四个选项中,只有一个选项是最符合题目要求的。
27. 下列变化中,属于物理变化的是
A. 蜡受热熔化 B. 植物的光合作用
C. 生石灰遇水放出大量热 D. 鸡蛋变臭
28. 下列各组物质中,前者为混合物,后者为单质的是
A. 食盐水、碘酒 B. 液态氧、空气
C. 石油、硫磺 D. 氧化镁、木炭
29. 下列物质的用途,只利用了其物理性质的是
A. 干冰用于人工降雨 B. 稀硫酸用于除铁锈
C. 氧气用于炼铁 D. 熟石灰中和土壤的酸性
30. 化学肥料通常所说的“含氮量”中的“氮”是指
A. 氮分子 B. 氮原子
C. 氮离子 D. 氮元素
31. 保护环境就是保护人类赖以生存的家园。下列做法不利于环境保护的是
A. 分类回收垃圾 B. 天然气代替煤作燃料
C . 污水处理后排放 D. 焚烧废旧塑料袋
32.下列说法中正确的是
A. 当给饱和溶液降低温度时,一定有晶体析出
B. 溶液中只能含有一种溶质
C. NaOH溶液敞放在空气中质量会增重并发生化学变化
D. 搅拌既可以使固体物质加快溶解,还能使其溶解度增大
33. 手机使用的锂(Li)电池是新型的高能电池,某种锂电池的总反应可表示为 Li+MnO2=LiMnO2。此反应中锂元素的化合
价变化为0→+1,下列对锰元素的化合价变化判断正确的是
A. +4→+3 B. +2→+3
C. 0→+2 D. -4→-2
34. 将20℃时的硝酸钾饱和溶液升温至50℃(不考虑水分的蒸发),一定发生改变的是
A. 硝酸钾的溶解度 B. 溶液的质量
C. 溶质的质量分数 D. 溶质的质量
35.发射“神舟五号”飞船的火箭所用的燃料燃烧时的化学方程式为
C2H8N2+2N2O4=3R+2CO2+4H2O,则R的化学式为
A. N2 B. NO
C. NO2 D. N2H4
36. 在食盐中混有少量的硫酸镁,若同时除去Mg2+和SO42-,应加入的试剂是
A. Ba(NO3)2 B. Ba(OH)2
C. K2CO3 D. KOH
37. 氢气是一种绿色能源,科学家们最新研制出利用太阳能产生激光,再用激光使海水分解得到氢气的新技术,其中海水分解可
以用化学方程式表示为 ![]()
下列说法不正确的是
A. TiO2在反应中作还原剂 B. 水分解不产生污染物
C. TiO2在反应中作催化剂 D. 该技术可以将太阳能转化为氢能
38. 下列各组溶液中,不用其他试剂仅用组内物质相互反应就能区别开来的是
A. CuSO4、NaOH、NaCl、Ba(NO3)2 B. NaCl、Na2CO3、KNO3、HCl
C. Na2SO4、K2CO3、KNO3、Ba(NO3)2 D. FeCl3、NaOH、KCl、Na2SO4
化 学(共39分)
相对原子质量: O—16 H—1 Fe—56 S—32
|
得分 |
评卷人 |
|
|
|
七、填空题(本大题包括5个小题,共20分)
59. (4分)用数字和化学符号表示:
(1)两个氮原子_______________; (2)两个氢分子_______________;
(3)两个氯离子_______________; (4)两个碳酸根离子______________。
60. (2分)配平化学方程式:
□P+□O2![]() □P2O5
□P2O5
61.(4分)有H、O、C、N四种元素,选择适当的元素,组成符合下列要求的物质,将化学式填入空格内:
(1)清洁无污染的燃料,它是一种单质__________;
(2)在冶金工业中常用来作还原剂的氧化物是__________;
(3)与生命密切相关且占人体总质量2/3的液态物质__________;
(4)常用的一种氮肥,它是一种盐__________。
62.(4分)肯德基等“洋快餐”被查出含有致癌物质“苏丹红一号”,目前全球多数国家都禁止将其用于食品生产。它的
化学式为C16H12N2O,它属于______________(填“无机物”或“有机物”),每个分子中共有______________个原子,其中
氧元素和氢元素的质量比为______________。
63.(6分)阅读下列材料,回答有关问题:
2002年中国消协对部分装修后的室内环境状况进行抽样测试发现,近半数存在苯污染,国际卫生组织已把苯定为强烈致癌
物质。苯在常温下是一种没有颜色带有特殊气味的液体,密度比水小,不溶于水。其化学式为C6H6,苯能在空气中燃烧生成二氧
化碳和水。请回答:
(1)苯的物理性质:_________________________________________________________;
(2) 苯的化学性质:_________________________________________________________;
(3) 写出苯在空气中燃烧的化学方程式:_____________________________________;
(4)化工原料店应如何保存苯?_____________________________________________。
|
得分 |
评卷人 |
|
|
|
八、实验题(本大题共13分)
64. (9分)在学习了二氧化碳的性质后,某同学在家里做如下图所示实验。根据图示回答下列问题:
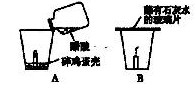
(1) 在A中观察到的主要现象是:①_________________________________________;
②_____________________________________________________________。由上述现象可得CO2具有的性质是
___________________________________________________________。根据上述性质可以确定CO2的一个主要用途是_
______________________________________。
(2) 当蜡烛熄灭后,在玻璃杯上迅速盖上一块蘸有澄清石灰水的玻璃片,如上图B,观察到的现象是
___________________________________________________________,写出有关反应方程式:
_____________________________________________________________。
(3) 根据B中的现象能否证明蜡烛中是否含有碳元素?________________。为什么?
__________________________________________________________________________。
65.(4分) 实验室提供下列盛有药品的仪器,某实验小组通过实验证明某一混合气体中含有二氧化碳、一氧化碳和水蒸气。
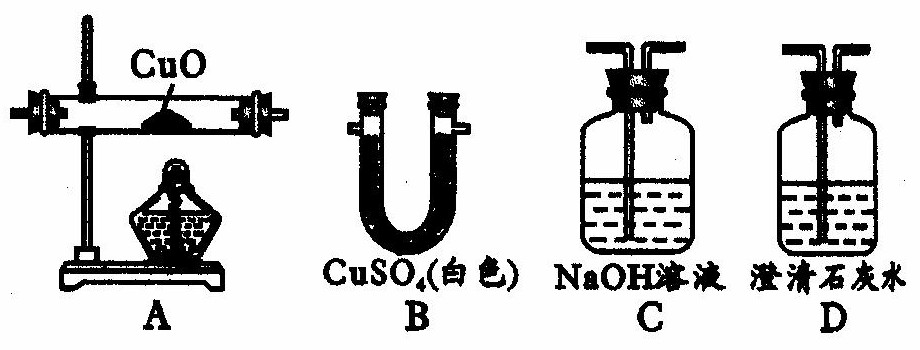
用A、B、C、D填空:
(1) 现分别证明混合气体中含有某一种气体,
① 若证明其中含有二氧化碳,应选用_____________________。
② 若证明其中含有水蒸气,选用__________________________。
(2) 选择必要的仪器(每种只用一次)证明其中含有CO,按气体通过的先后顺序是:
______________________________________。
|
得分 |
评卷人 |
|
|
|
九、计算题(本大题共6分。计算结果精确到1%)
66. 甲、乙、丙三位同学分别取铁粉和铜粉的均匀混合物与某稀硫酸反应,所得数据如下:
|
|
甲 |
乙 |
丙 |
|
取用金属混合物的质量(g) 取用稀硫酸的质量(g) 反应后过滤得到干燥的固体的质量(g) |
10 100 2 |
10 120 2 |
20 100 12 |
计算:(1)金属混合物中铁的质量分数;
(2)甲制得的硫酸亚铁溶液中溶质的质量分数。
沐川县初中2006届二调考试
化学参考答案
一、选择题:每题3分,共36分。
|
题号 |
27 |
28 |
29 |
30 |
31 |
32 |
33 |
34 |
35 |
36 |
37 |
38 |
|
答案 |
A |
C |
A |
D |
D |
C |
A |
A |
A |
B |
A |
A |
七、填空题,共20分。
59.(1)2N (2)2H2 (3) 2Cl- (4)2CO32- (4分,每空1分)
60.4 5 2 (2分)
61.(1) H2 (2)CO (3)H2O (4)NH4NO3 (4分,每空1分)
62. 有机物 31 4:3 (4分,1、1、2分)
63.(1) 没有颜色带有特殊气味的液体,密度比水小,不溶于水。 ( 1分 )
(2) 有可燃性(或能在空气中燃烧生成二氧化碳和水) ( 1分 )
(3) ( 2分 )
(4) 密封保存干阴凉处,注意避免火源 ( 2分 )
八、实验题,共13分。
64. (1)① 鸡蛋壳逐渐溶解,有气泡产生 ② 蜡烛火焰熄灭
不支持燃烧 用于灭火 (4分,每空2分)
(2)变浑浊 Ca(OH)2+CO2=CaCO3↓+H2O (3分,1分、2分)
(3)不能 因为CO2来自于两方面:① 蜡烛燃烧产生,②鸡蛋壳与醋酸反应产生 (2分,每空1分)
65. (1)① D ② B (2分,每空1分)
(2)C→B→A→D ( 2分 )
九、计算题,共6分。
66. 解:由题给条件分析知道,甲用的金属混合物刚好与酸完全反应。
参加反应的Fe为10-2=8g,设生成硫酸亚铁的质量为x,产生氢气的质量为y。
56 152 2 8g x y
Fe + H2SO4 = FeSO4 + H2↑ (1分)
56∶152=8g∶x x≈21.7g (1分)
56∶2 =8g∶y x≈0.3g (1分)
(1)金属混合物中铁的质量分数为:8/10=0.8=80% (1分)
(2) 甲制得的硫酸亚铁溶液中溶质的质量分数为:21.7/(8+100-0.3)≈0.20=20% (2分)
答:略。
