理 化
第Ⅰ卷 (选择题 共75分)
一、本卷共14小题。每小题2.5分,共35分。下列各题的四个选项中,只有一个选项是最符合题目要求的。
1.2008年初,一场历史罕见的大范围低温雨雪冰冻袭击了中国南方部分省市,此次雪灾给我国造成了巨大的经济损失。下列说
法正确的是
A. 雪是一种单质 B. 当雨雪成为冰冻时,分子的运动就停止了
C. 冰和雪的主要成分都是水 D. 冰雪融化的过程是一种化学变化
2.下列家庭常用的调味品中,可视为纯净物的是
A. 食醋 B.白糖
C. 食盐 D.白酒
3.2008年5月17日,在“5.12汶川大地震”抗震救灾现场,中国疾病预防控制中心的防疫人员受到了胡锦涛总书记的接待,当
时他们正在喷洒“含氯消毒液”。“含氯消毒液”中的“氯”在这里是指
A.元素 B.分子
C. 原子 D. 离子
4.下表是某同学制定的食谱单,为使营养均衡,在“你的补充”栏可以选填的食物是
|
主食 |
米饭、 馒头 |
|
菜肴 |
清蒸鱼、红烧鸡肉、花生米 |
|
乳品 |
牛奶 |
|
你的补充 |
|
A.油炸大虾 B.红烧豆腐
C.皮蛋 D.凉拌黄瓜
5.国家环保部确定,2008年6月5日世界环境日的中国主题为“绿色奥运与环境友好型社会”。下列做法不符合该主题的是
 A. 拒绝使用一次性塑料餐饮具
A. 拒绝使用一次性塑料餐饮具
B.草坪绿化采用微灌或滴灌智能控制技术
C. 投入大量明矾和消毒剂处理受污染的河水
D.尽可能使用电动汽车和开发新型清洁燃料汽车
6.下列区别物质的方法错误的是
A.用肥皂水区别软水和硬水 B.用熟石灰区别尿素和硝酸铵
C.用燃烧的方法区别羊毛和涤纶 D.用酚酞溶液区别稀盐酸和食盐溶液
7.向滴有酚酞的NaOH溶液中逐渐滴入稀盐酸至过量,下面叙述正确的是
A.溶液由无色变为红色,pH逐渐减小 B.溶液由红色变为无色,pH逐渐增大
C.溶液颜色不变,pH逐渐增大 D.溶液由红色变为无色,pH逐渐减小
8.2008年6月1日起,全国执行“限塑令”。某市组织宣传活动,发放无纺布袋。生产无纺布的主要原料为:聚丙烯、聚酯和黏
胶等。下列有关说法错误的是
A.大部分塑料在自然环境中很难降解 B.使用无纺布袋有利于减少“白色污染”
C.生产无纺布与棉布的原料都是天然纤维 D.聚乙烯、聚丙烯、聚酯都属于合成材料
9.下图是用比例模型来表示物质间发生化学变化的微观示意图。图中![]() 和
和![]()
分别表示两种元素的原子,能用该图示表示的化学反应是
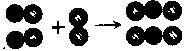
A.2H2+O2 2H2O B.2CO+02
2CO2
C.CO2+H2O=H2CO3 D.H2+Cl2 ![]() 2HCl
2HCl
10.20℃时,分别向盛有10g水的两支试管中加入等质量的甲、乙两种物质,使其充
分溶解,可观察到如下图1所示的现象。下列说法正确的是
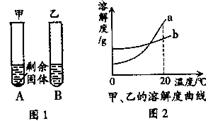
A.20℃时B试管中的溶液一定是饱和溶液 B.图2中b表示甲物质的溶解度曲线
C.降温可使A试管中剩余的固体继续溶解 D.甲物质的溶解度一定比乙物质小
11.比较及推理是化学学习和研究中常用的思维方法。以下是根据一些反应事实推导出的
影响化学反应的因素,其中推理不正确的是
|
序号 |
化学反应事实 |
影响化学反应因素 |
|
A |
铁丝在空气中很难燃烧,而在氧气里能剧烈燃烧 |
反应物的浓度 |
|
B |
碳在常温下不与氧气发生反应,而在点燃时能与氧气反应 |
温度 |
|
C |
双氧水在常温下较难分解,而在加入二氧化锰后迅速分解 |
催化剂 |
|
D |
铜片在空气里很难燃烧,铜粉在空气里较易燃烧 |
反应物的种类 |
12. 某同学先经实验研究,后归纳得出以下两个事实:①在高温条件下,木炭不能用来还原铝矿,但可用来还原铜矿和铁矿;
②不能用铁制容器盛放硫酸铜溶液。根据以上情况推知,C、Al、Cu、Fe四种元素的活动性由强到弱的顺序是
A. Al>C>Fe>Cu B. C>Al>Cu>Fe
C. Al>C>Cu>Fe D. C>Fe>Al>Cu
13. 媒体报道,目前家居环境的空气污染主要是装修时所用的油漆中含超量的甲醛(化学式为CH2O)所致,下列关于甲醛的说
法正确的是
A. 甲醛是氧化物 B. 甲醛分子中氢原子和氧原子的个数比是2:1
C. 可以用甲醛水溶液来浸泡鱿鱼 D. 甲醛由碳、氢、氧三个元素组成
14.只需加水就可将四种白色固体鉴别出来:(1)NaCl、(2)BaCl2、(3)CuSO4、(4)Na2SO4,正确的鉴别顺序是
A. (1)(3)(4)(2) B.(1)(2)(3)(4)
C. (3)(2)(4)(1) D.(3)(4)(2)(1)
第Ⅱ卷 (非选择题 共35分)
可能用到的相对原子质量: Ca─40 O─16 C─12 H─1 Cl─35.5
|
得分 |
评卷人 |
|
|
|
二、填空题(本大题包括5个小题,每空1分,共16分)
31.通过“常见的酸和碱”的学习,我们认识了酸和碱。常见的酸有硫酸、盐酸等,在它们的水溶液里由于存在相同的
(填符号),因此它们具有很多相似的化学性质,如 (写一条即
可)。
32. 食物中的糖类给人体提供热量,某糖在人体内发生反应是C6H12O6+6O2 ![]() 6CO2+6X,则X的化学式为 。
6CO2+6X,则X的化学式为 。
33. 2008年北京奥运会上,体操运动员在做器械体操时,总要先站在场地旁边,在手掌上擦抹一种白色的粉末。该物质叫“镁
粉”,化学名称叫碳酸镁,具有吸水性。
(1)镁的化学式是 ,所属物质类别是 ;
(2)碳酸镁在加热时可生成氧化镁和二氧化碳,写出反应的化学方程式 ,该反应所属的基本
类型是 ;
(3)运动员上场后,双手插入盛有“镁粉”的盆中擦擦手心,其作用是 。
34.2008年9月,国家食品管理局通报了三鹿等22家企业非法在奶粉中添加三聚氰胺的行为。已知三聚氰胺的化学式为C3N6H6,
白色晶体,无味,在常压下,300℃升华,354℃分解,微溶于水,水溶液呈弱碱性,能够与各种酸反应。
(1)根据以上信息,请你总结出三聚氰胺的性质:
物理性质: ;
化学性质: ;
(2)要检验三聚氰胺呈碱性,可用的试剂是 ,现象为 。
35. 某自来水厂用源水处理成自来水的流程如下,请分析:
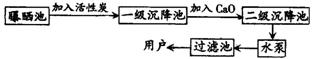
(1)在乡村没有活性炭,常加入 来净水;
(2)静置、吸附、过滤、蒸馏等实验操作中,可以降低水的硬度的是 ;
(3)若该地区源水中含有较多的MgCl2,写出在源水处理流程中加入CaO时的化学方程式:① ,
② 。
三、实验与探究(本大题共2小题,共11分)
36. 有下列实验仪器(下左图):
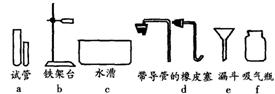
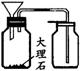
(1)其中名称有错误的是 (填序号字母);
(2)用氯酸钾制取氧气,还需要补充的玻璃仪器是 ;
(3)若用上右图装置制取CO2,需要太多的稀盐酸才能淹没漏斗的下端管口,起到液封的作用。请在左图中选择一种仪
器,加在右图装置上来解决该问题。请把该仪器画在图中应该放置的位置。
37. 某研究性学习小组发现:通常检验CO2用饱和石灰水,吸收CO2用浓NaOH溶液。
在体积相同盛满CO2的两个集气瓶中,分别加入等体积的饱和石灰水和浓NaOH溶液。实验装置和现象如下图所示。
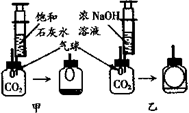
(1)写出甲装置中发生的化学反应方程式: ;
(2)实验中能表明通常用石灰水而不用NaOH溶液检验CO2的实验现象是 ;
(3)能表明用NaOH溶液吸收CO2比用石灰水吸收CO2效果更好的实验现象是 。用你学到的
化学知识,分析其中的原因: 。
四、计算题(本大题共8分,计算结果精确到1%)
38. 有一种石灰石样品的成分是CaCO3和SiO2,课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水),得到如下部分数据和图象。请计算:
|
次数 |
第1次 |
第2次 |
第3次 |
|
加入盐酸的质量/g |
20 |
20 |
20 |
|
剩余固体的质量/g |
30 |
a |
20 |
(1) CaCO3中钙、碳、氧三种元素的质量比是 ;
(2)第2次加入盐酸后,a为 g;
(3)原混合物中CaCO3的质量分数;
(4)第4次加入盐酸完全反应后,所得溶液中溶质的质量分数。
沐川县初中2009届第二次质量检测
化学试题参考答案
一、选择题。35分,每题2.5分。
|
题号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
答案 |
C |
B |
A |
D |
C |
D |
D |
|
题号 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|
答案 |
C |
B |
B |
D |
A |
B |
C |
二、填空题。16分,每空1分。
31. H+ 与碱反应生成盐和水(或其它正确答案)
32. H2O
33. (1)Mg 单质 (2)MgCO3 ![]() MgO+CO2↑ 分解反应
MgO+CO2↑ 分解反应
(3)利用吸水性。增大手与器械之间的摩擦,便与握紧。
34. (1)物理性质:白色晶体,无味,在常压下,300℃升华,微溶于水。
化学性质:354℃分解,能够与各种酸反应。
(2)酚酞试液(或pH试纸) 酚酞试液变红(或pH>7)
35. (1)木炭 (或其它正确答案也可) (2)蒸馏
(3)CaO+H2O=Ca(OH)2 Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓
三、实验与探究。11分。
36. (1)c f (2分) (2)酒精灯 (1分) (3) ![]() (2分)
(2分)
37. (1)CO2+ Ca(OH)2=CaCO3↓+H2O (2分)
(2)石灰水变浑浊而氢氧化钠溶液不变浑浊 (2分)
(3)乙装置中的气球比甲装置中的气球涨得更大 Ca(OH)2的溶解度小,所能配制的饱和溶液的浓度小(或其它正确答案也可)
(2分)
四、计算题。8分
38. (1)10:3:12 (2分)
(2)25 (1分)
(3)20/35×100%≈57% (1分)
(4)设反应后制得CaCl2 的质量为x,生成CO2的质量为y。
CaCO3+2HCl= CaCl2+ H2O+ H2O↑
100 111 44
20g x y
100:111= 20g: x x=22.2g (1分)
100:44 = 20g: y y=8.8g (1分)
反应后溶液中溶质的质量分数为:22.2/(20+80-8.8)×100%≈24% (2分)
答:反应后溶液中溶质的质量分数为24%。
