编题:卢老师(选自2003年常州、南京、南通中考试题)
可能用到的相对原子质量:H—1 C—1 2 O—1 6 Fe—5 6
一、选择题(本题包括10小题,共20分。每小题只有一个选项符合题意,请将答案写在下表中。)
1
2
3
4
5
6
7
8
9
10
1.在下列过程中,没有发生化学变化的是( )。
(A)酒精挥发 (B)食物腐败 (C)钢铁生锈 (D)碳铵分解
2.下列关于空气的叙述,错误的是( )。
(A)空气中最多的气体是氮气
(B)空气是由多种单质和多种化合物组成的混合物
(C)空气中二氧化碳的含量是始终不变的
(D)空气是一种重要的化工原料
3.以下生活、学习经验,不能说明分子间有空隙的是( )。
(A)打气筒能将气体压缩 (B)酒精和水混合后,总体积变小
(C)物体有热胀冷缩的现象 (D)海绵能吸水
4.食盐、食醋、纯碱等均为家庭厨房中常用的物质,利用这些物质你能完成的实验是( )
①检验自来水中是否含氯离子 ②鉴别食盐和纯碱 ③检验鸡蛋壳能否溶于酸④除去
热水瓶中的水垢
A.①② B.①③ C.①④ D.②③④
5.现榨的苹果汁在空气中会由淡绿色变为棕黄色。你猜测其原因可能是( )
A.苹果汁中的Fe2+变成Fe3+ B.苹果汁中含有Cu2+
C.苹果汁中含有OH- D.苹果汁中含有K+
6.正常雨水与酸雨的差异是( )。
(A)正常雨水显中性,酸雨显酸性
(B)正常雨水的pH约为5.6,酸雨的pH<5.6
(C)正常雨水不含杂质,酸雨含杂质
(D)正常雨水降在农村,酸雨降在城市
7.下列实验操作后,溶液温度会升高的( )。
①浓硫酸倒入水中 ②氢氧化钠固体溶于水中 ③生石灰放入水中
④浓盐酸滴入浓烧碱溶液中 ⑤氯化钠晶体溶于水中 ⑥硝酸铵晶体溶于水中
(A)只有①②③ (B)只有①②③④
(C)只有①②③④⑤ (D)有①②③④⑤⑥
8.在滴有紫色石蕊试液的氢氧化钠溶液里慢慢滴加稀盐酸至过量,溶液的( )。
(A)颜色由蓝色变成红色 (B)颜色由红色变成蓝色
(C)颜色由蓝色变成紫色 (D)pH慢慢降至7
9.若将一定质量的硝酸钾不饱和溶液变为饱和溶液,则( )。
(A)溶液的质量一定变小 (B)溶液中溶质的质量分数一定变大
(C)溶液的质量一定变大 (D)溶液中溶质的质量分数可能不变
10.一定温度下某物质的溶解度为20g,在该物质的饱和溶液中,溶质、溶剂、溶液的质量比为 ( )。
(A)1:5:6 (B)1 : 4:5 (C)20:1:21 (D)5:1:6
二、填空题(本题共17分)
11.干冰可用于人工降雨,干冰的化学式为 。医疗上常用体积分数为70%~75%的乙醇溶液作消毒剂,乙醇的化学式为 。
12.目前市场上销售的汽水饮料大多数是碳酸饮料,其中溶有二氧化碳气体。打开汽水瓶盖时,汽水会自动喷出来。这说明气体在水中的溶解度与 有关。喝了汽水后,经常会打嗝。这说明气体的溶解度还与 有关。
13.先在表中空白处填写相关的内容,再根据表中提供的信息研究下面的问题。
反应物I
反应物Ⅱ
反应现象
说 明
AgNO3溶液
NaCl溶液
生成白色沉淀
该沉淀为AgCl,不溶于稀H NO3
BaCl2溶液
Na2SO4溶液
生成白色沉淀
该沉淀为BaSO4,不溶于稀HCl
Na2CO3溶液
生成白色沉淀
该沉淀为 ,溶于稀HCl
由蒸发海水制得的食盐中,常含有Na2SO4、CaCl2等杂质,这些杂质对后继生产有害,需要除去。问:
(1)Na2SO4和CaCl2在溶液里能形成Na+、SO42-、Ca2+和Cl-四种离子。要除去其中的Ca2+,可使用 溶液;除去其中的SO42-,可使用 溶液。
(2)在工业生产的除杂过程中,又会带进CO32-和OH-。要同时除去这两种杂质离子,最简便的方法是加入适量的 ,并用 测定溶液的酸碱性。
14.为了履行国际社会的《关于消耗臭氧层物质的蒙特利尔议定书》,我国政府决定自2003年6月1日起在全国范围内禁止使用“CTC"作为清洗剂。“CTC"又称作四氯化碳,是常用的服装干洗剂,也是修正液(又称涂改液)中的一种溶剂,还是.一种优良的灭火剂。根据以上信息回答:
(1)“CTC"的化学式为 ,其中碳元素的化合价为 。
物理性质:
化学性质: 。
15. “物质的组成与结构决定物质的性质”是化学科学中的重要观点。按照这一观点讨论下面的问题。
酸溶液具有一些共同的化学性质,是因为酸溶液中都含有 离子;碱溶液也具有一些共同的化学性质,是因为碱溶液中都含有 离子。因此,酸溶液与碱溶液反应一定能生成 。
三、实验题(本题共7分)
16.实验室提供以下常用仪器,供完成下列气体制取实验时选用(不可重复选用)。
(1)实验室采用加热高锰酸钾晶体制取O2时,其发生装置必需选用上述仪器中的(填写序号,下同) ,还缺少的仪器是 。
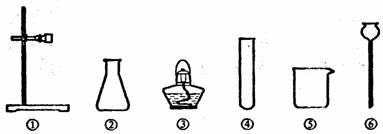
(2)过氧化氢(H2O2)俗称双氧水,常温下是一种无色液体, 它在土豆块的催化作用下能迅速分解,放出氧气。若实验室采用该反应原理制取O2 ,并且在实验过程中可以随时添加双氧水,上述仪器中必需使用的有 ;试写出此反应的化学方程式: 。
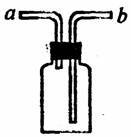 (3)若直接使用右图所示装置收集O2,O2由 口进入;若将装置中布满水,O2由 口进入。该装置除收集气体外,还可用作 。
(3)若直接使用右图所示装置收集O2,O2由 口进入;若将装置中布满水,O2由 口进入。该装置除收集气体外,还可用作 。
四、计算题:(本题共6分)
17.“骨质疏松症”是由人体缺钙引起的,可服用补钙剂来治疗。乳酸钙(CaC6H12O6·5H2O)是一种常见的补钙剂,市售乳酸钙片剂每片含乳钙200mg,一个成.年人缺钙病人天天服用20片乳酸钙片剂可达到补钙目的。
计算:(计算结果保留整数)
(1)乳酸钙中各元素的质量比 。
(2)该成年缺钙病人改用喝牛奶(每100mL牛奶中含钙≥O.104g)来补钙,天天至少需喝 毫升牛奶。
18.生铁和钢都是铁合金,生铁中碳的含量在2.O%~4.3%之间,钢中碳的含量在O.03%~2.O%之间。将一块质量为10.Og的铁合金放入锥形瓶中,再向锥形瓶中加入100g稀H2SO4,恰好使铁合金中的铁完全反应(碳不溶于稀H2SO4;铁合金中其他元素含量很低,可忽略不计),测得生成H2的体积为4.00L(H2在该条件下的密度为O.0880g/L)。
试根据计算回答:(计算结果保留三位有效数字)
(1)该铁合金是生铁还是钢?
(2)反应后所得溶液的溶质质量分数。
