第一部分
(可能用到的原子量:H—1 C—12 N—14 O—16 Na—23 S—16 Cl—35.5 K—19 Fe—56 Cu—64 Zn—65 Ag—108)
一、选择题(每题2分,共40分)
1、 下列变化属于化学变化的是( )
A、从空气中分离出氧气 B、铁块熔化成铁水
C、铁生锈 D、干冰升华
2、下列物质中,属于混合物的是( )
A、盐酸 B、液态氧 C、二氧化碳 D、高锰酸钾
3、空气的成分按体积分数计算,含量最多的是( )
A、氧气 B、氮气 C、二氧化碳 D、稀有气体
4、判定铁在氧气中燃烧是化学反应的主要依据是( )
A、发出刺眼的白光 B、放出大量的热
C、有黑色固体物质生成 D、剧烈燃烧
5、氧气可以用排水法收集的原因是( )
A、比水的密度小 B、比空气的密度大
C、不与水反应,也不易溶于 D、水中含有氧气
6、下列现象不属于分子运动的是( )
A、汽油挥发 B、湿衣服晾干
C、蔗糖溶于水中 D、火药爆炸
7、能保持氢气化学性质的微粒是( )
A、氢分子 B、氢原子 C、氢元素 D、氢离子
8、下列物质的化学式与名称一致的是( )
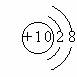
A、氧化镁MgO2 B、二氧化硫O2S
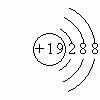 |
C、氯气Cl2 D、锰酸钾KMnO4
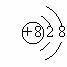 |
 | ||
9、某元素X的最外层有3个电子,某元素Y的最外层有6个电子,这两种元 素组成的化合物的化学式可能是( )
A、X2Y3 B、XY C、Y3X2 D、X3Y2
10、质量守恒定律的适用范围是( )
A、实验室里发生的反应 B、自然界里发生的反应
C、工业生产中发生的反应 D、在自然界里发生的所有化学反应
11、下列物质不属于合金的是( )
A、生铁 B、白口铁 C、氯化铁 D、球墨铸铁
12、铁片放入下列哪种溶液,铁片质量减轻( )
A、CuSO4溶液 B、稀H2SO4溶液
C、AgNO3溶液 D、ZnSO4溶液
13、下列物质属于溶液的是( )
A、冰水 B、牛奶 C、碘酒 D、石灰浆
14、某饱和溶液降低温度时,有晶体析出,此时溶液( )
A、仍是饱和溶液 B、溶质的质量分数不变
C、溶液的质量不变 D、溶质的质量分数增大
15、下列物质的水溶液,不能导电的是( )
A、食盐晶体 B、蔗糖溶液
C、氢氧化钠晶体 D、硫酸
16、下列物质中,溶于水后其溶液的pH值最小的是( )
A、食盐 B、硫酸钠 C、二氧化碳 D、生石灰
17、酸、碱、盐三类物质的相同点是( )
A、都含有氢元素 B、都含有氧元素
C、都能溶于水 D、都不是单质
18、下列物质长期敞口放置在空气中,质量会增加,且有新物质产生的是 ( )
A、硫酸钡 B、浓硫酸 C、浓盐酸 D、苛性钠
19、下列电离方程式书写正确的是( )
A、MgCl2==Mg 2 2Cl- B、Na2SO4==Na2 SO42-
C、HNO3==H NO3- D、KClO3==K Cl- 3O2-
20、下列物质的制备,能由一步反应实现的是( )
A、KNO3→KOH B、Fe2O3→Fe(OH)3
C、Cu→Cu(NO3)2 D、CaCO3→Ca(OH)2
二、填空题(每空1分,共24分)
21、用数字和化学符号表示:
(1)两个氢原子______ (2)三个氮分子________
(3)五个碳酸根离子________
22、根据下列微粒结构示意图,回答问题。
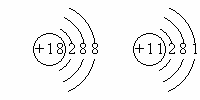 |
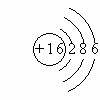 |
A B C D E F
1)表示金属元素原子的是_________;
2)表示非金属元素原子的是_______;
3) 表示稀有气体元素原子的是________;
4)表示稳定结构的是____________。
23、 在H2、O2、CO2、Ca(OH)2、盐酸、酒精、高锰酸钾中,常用于抢救病人
的是____________,用于除去铁器表面铁锈的是________,可用来改良酸性土壤的
是_________,属于有机物中的绿色能源的是_________,既可用于实验室制氧气,又可用于消毒的是________。
24、20℃时,把18克氯化钠溶解在50克水里,恰好制成饱和溶液,则20℃时氯化钠的溶解度为_______克,该饱和溶液中氯化钠的质量分数为________。
25、 氢氧化钠必须密封保存,因为它不仅能吸收空气里的_______,而且还能与空气中的________反应而变质,其反应方程式为_________________________。
26、 生铁和钢都是铁合金,其中含碳量_______较多,为_______。据有关资料统计得到每年钢铁锈蚀的量是当年生产总量的1/4,钢铁生锈的原因是由于铁与____和_____反应所造成的。
27、一氧化氮是大气污染物之一。目前,有一种治理的方法:在400℃左右,有催化剂存在的情况下,用氨气和一氧化氮反应生成氮气和水,请写出该反应的化学方程式_______________________________。
28、浓硫酸不与铁发生置换反应,在工厂里常用铁罐盛装浓硫酸。但近年来,一些个体修配厂的电焊工人在焊接用水清洗过的盛装浓硫酸的铁罐时,却发生了多起爆炸事故。请写出引起爆炸事故的两个化学方程式:
1)_________________________;
2)________________________。
三、实验题(每空1分,共10分)
29、量筒、试管、漏斗、玻璃片分别是下列实验中的一种必用仪器,将其名称填入下表相应的空格内。
实验操作
过滤
氢气还原氧化铜
配制一定质量分数的溶液
排水法收集一瓶氧气
必用仪器
30、在没有现成CO2气体发生器的情况下,请你选用下图中的部分仪器,装配成一个简易的能随开随用、随关随停的CO2气体发生装置。
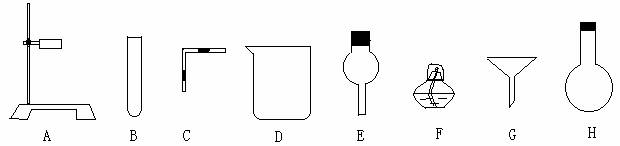
(1)写出A、B、F的仪器名称A______ B______ F______
(2)若装配一套装置,应选用的仪器是_______________。(用四种仪器代号填写)
(3) 若用上述装置制取CO2气体,而实验室里只有稀硫酸、盐酸、水、块状纯碱、块状大理石,按照比较合理的方案,则应选用的药品是
_______________,反应的化学方程式为_______________________。
四、计算题(31题2分,32题4分)
31、酸牛奶中含有的乳酸的化学式为C3H6O3,其中C、H、O原子个数比为___________,式量为________。
32、硫酸钠与碳酸钠的固体混合物12.2克与150克稀硫酸恰好完全反应生成正盐,同时生成2.2克气体,求混合物中碳酸钠的质量分数。
第二部分
(1—4小题中每题有1—2个答案,选择题每题2分,其余每空1分)
1、地球外层空间存在着微量的臭氧(O3)和氧原子,该臭氧层的存在能吸收和阻挡太阳光中有害的强烈紫外辐射。可是人为的大气污染物会破坏臭氧层,如超音速飞机、排放物中的氮氧化物(NO和NO2),它们和O3和O发生如下反应:O3 NO==NO2 O2;O NO2==NO O2,这两个反应反复循环,以下说法正确的是( )
A、以上反应的总反应式是:O3 O==2O2
B、以上反应的总反应式是:2O3==3O2
C、以上的反应使NO的量逐渐减小,NO2的量逐渐增加
D、以上反应中NO起催化作用
2、目前学生们喜欢使用涂改液,经实验证实涂改液中含有许多挥发性有害物质,吸入后易引起慢性中毒而头晕、头痛,严重者抽搐,呼吸困难。二氯甲烷就是其中的一种,下列关于二氯甲烷(CH2Cl2)的几种叙述中正确的是( )
A、它是由碳、氢、氯三种元素组成的化合物
B、它是由氯气和甲烷组成的混合物
C、它的分子中碳、氢、氯元素的原子个数比是1:2:2
D、它是由多种原子构成的一种化合物
3、炼钢炉中有一化学反应:FeO C===Fe CO↑,对该反应说法不正确的是( )
A、该反应为氧化还原反应 B、一氧化碳为还原剂
C、氧化亚铁为氧化剂 D、碳发生了还原反应
4、取式量为46的某有机物4.6克,在足量的氧气中充分燃烧,生成8.8克二氧化碳和5.4克水,据此判定该有机物( )
A、只由碳、氢两种元素组成
B、一定含碳、氢、氧三种元素
C、其分子中碳、氢、氧原子个数比为2:6:1
D、其化学式为CH2O2
5、 铜绿的主要成分是碱式碳酸铜[Cu2(OH)2CO3],它能跟酸反应生成铜盐、水和二氧化碳。某同学用小刀从旧制铜器上刮下铜绿,用来制取铜。请回答:
(1)下面方框图表示制取的步骤和方法,请在方框内填上所制物质的化学式。
H2SO4 NaOH △ H2,△
铜绿
① ② ③ ④
(2)写出步骤①反应的化学方程式:_________________________________。
(3)若实验装置及在生成铜以前的操作都正确,但最后结果没有铜生成,这是因为______________________________________________________。
6、录象用的高性能磁粉,主要材料之一是由三种元素组成的化学式为CoxFe3-xO3 x的化合物。已知其中氧元素为-2价、钴(Co)和铁可能呈现 2价或 3价。且上述
化合物中,每种元素只有一种化合价,则x值为_______,铁的化合价为________, 钴的化合价为_______。
7、为了对氯化钾样品(含有少量KNO3)进行组分分析,甲、乙、丙三位同学分别进行实验,他们的实验数据如下,请仔细观察分析,回答下列的问题:
甲
乙
丙
所取固体样品的质量(克)
20
10
10
加入AgNO3溶液的质量(克)
100
100
150
反应后所得的沉淀质量(克)
14.35
14.35
14.35
(1)三位同学中,哪一位同学所用的KCl与AgNO3刚好完全反应________。
(2)三位同学分别把反应后的溶液过滤,______同学所得的滤液是只含有一种溶质的溶液。此溶液的溶质质量分数是_______。
