试题说明:1.本试卷满分100分。
2.可能用到的相对原子质量:
H∶1 C∶12 N∶14 O∶16 Na∶23 S∶32 Cl∶35.5 Ca∶40 Cu∶64 Fe∶56 Zn∶65 Al∶27
3.考试时间:2h
一、选择题(本题包括15个小题,每小题2分,共30分。每小题有1个或2个选项符合题意。若有两个答案的错1个不得分,漏选1个扣1分。)
1.将下列四种家庭常用的调味品分别放入水中,不能形成溶液的是( )
A.食盐 B.食用油 C.味精 D.蔗糖
2.下列符号中,既能表示一个原子,又能表示一种元素,还能表示一种物质的是( )
A.H2 B.O C.C60 D.Cu
3.食用下列方法处理过的食品,不会危及人体健康的是( )
A.用干冰冷藏的食品 B.用硫磺熏制的白木耳.粉丝等食品
C.用甲醛浸泡的海鲜 D.用工业用盐腌制的肉类食品
4.我国有些煤矿的坑道中具有丰富的可燃性气体。利用该可燃气可建成发电厂,这样既充分利用了能源,又保证了煤矿的安全生产。坑道中主要的可燃性气体是( )
A.H2 B.CO C.CH4 D.CH4和CO的混合气体
5.“绿色化学”是21世纪化学科学发展的重要方向之一,其核心是从源头上减少对环境的污染。你认为“绿色化学”是指化学工业生产中( )
A.对废气、废水、废渣进行严格处理
B.少用或不用有害物质以及少排或不排放有害物质
C.不使用任何化学物质
D.在化工厂种草、种树,使其成为花园式工厂
6.室内空气污染的主要来源之一是人们现代生活中所使用的某些化工产品,如有些装饰材料.化纤地毯.涂料等会不同程度地释放出某种气体,该气体可能是( )
A.氟利昂 B.二氧化碳 C.甲醛 D.甲烷
7.下列物质可以用作食品抗氧化剂的是( )
A.炭粉 B.铁粉 C.氯化钙 D.生石灰
8.人体内含有多种元素,其中许多元素都是人体所需的。但有些元素尚未证实其生理功能,在食品中它们的含量稍高会引起毒性反应。我国食品卫生法对这些元素在食品中的含量的最高标准有极严格的规定,这些元素是( )
①Na ②Mg ③As ④Cd ⑤Ca ⑥Zn ⑦Hg ⑧Pb ⑨Fe ⑩K
A.⑥⑦⑧⑨ B.②④⑥⑧ C.③④⑦⑧ D.②④⑥⑦⑧
9.某学生将食盐.生石灰.米醋.酸奶分别放入等质量的水中,逐一进行了PH的测定,并表示在下面的数轴上,其中能表示生石灰溶于水形成溶液的PH的是( )
![]()
10.当水的温度和压强升高到临界点(t=374.3℃,p=22.05MPa)以上时,水就处于超临界状态,该状态的水即称之为超临界水。超临界水具有通常状态下水所没有的特殊性质。它可以和空气.氧气及一些有机物质均匀混合。如果超临界水中同时溶有氧气和有机物,则有机物可迅速被氧化,生成二氧化碳.氮气.水等。有关超临界水的叙述错误的是( )
A.超临界水可处理有机废物 B.超临界水是一种新物质
C.超临界水是水的一种状态 D.超临界水氧化技术不形成二次污染
11.《美国化学会志》报道了中国科学家以二氧化碳和钠在一定条件下制得金刚石,其化学方程式为![]() (金刚石)。则X的化学式为( )
(金刚石)。则X的化学式为( )
A.Na2O2 B.Na2CO3 C.Na2O D.Na4C2O6
12.2002年诺贝尔化学奖得主之一的瑞士科学家维特里希夫巧妙地选用生物大分子中的某原子(X)作为测量对象,测出相邻X原子间的距离和方位。再通过计算机破译了某些生物大分子的空间结构。已知X原子是有机分子中数量最多的原子,该原子是( )
A.C B.H C.O D.N
13.有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如右图所示,则该溶液是( )
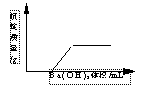
A.硝酸、硝酸铁 B.硫酸、氯化铁
C.盐酸、氯化铁 D.盐酸、硫酸铁
14.图表资料可以为我们提供很多信息。下面是某学生对图表资料的使用,其中正确的是( )
A.根据某元素的原子结构示意图判断该元素原子核中有几个中子
B.根据密度数据判断液体物质挥发性的大小
C.根据“各种物质在不同温度时的溶解度表”,设计通过蒸发.结晶把混合溶液中某些物质分离出来的方法
D.根据“相对原子质量表”判断每种元素原子中的质子数.中子数和核外电子数
15.把A.B.C.D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如下表所示:
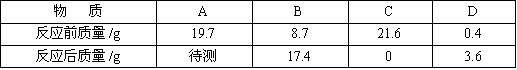
下列说法正确的是( )
A.物质C一定是化合物,物质D可能是单质
B.反应后密闭容器中A的质量为19.7g
C.反应过程中,物质B和物质D变化的质量比为87∶36
D.若物质A与物质C的相对分子质量之比为194∶216,则反应中A和C的化学计量数之比为1∶2
二、填空题(本题包括8个小题,共41分)
16.(3分)已知右图A.B.C三种元素的原子结构示意图依次为:
![]()
(1)X= ______, Y=________.。
(2)写出一种由A.B.C三种元素形成的化合物的化学式________。(用A.B.C代表元素符号)
17.(5分)某单位曾发生了一起亚硝酸钠中毒事件。亚硝酸钠外貌酷似食盐且有咸味,亚硝酸钠和食盐的有关资料如下:
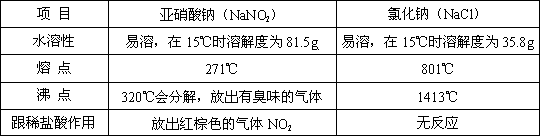
(1)根据上表,请你写出亚硝酸钠的两个物理性质:
① _________________________________________;
② ________________________________________。
(2)检验亚硝酸钠的方法可以是:______________________________
18.(4分)现有碳酸氢铵.硫酸钾两种固体化肥,请设计两种实验方法将它们加以区别。

19.(7分)在理解概念的基础上,理清概念之间的相互关系,构建知识网络是化学学习重要的学习方法。下图是初中常见化学概念之间的相互关系。
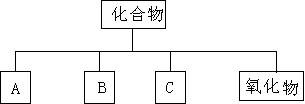
(1)写出A.B.C所属物质的类别,并以Na.H.O.S元素组成的物质为例各写出一种代表物质的化学式。
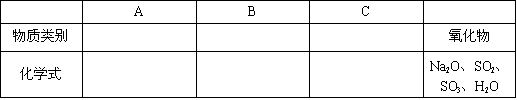
(2)NaHSO4是硫酸的酸式盐,NaHSO4的溶液具有酸性。写出NaHSO4与表中A.B.C.氧化物中某两种物质分别反应的化学方程式:
______________________________________________________
20.(5分)近年来,多次发生煤矿瓦斯爆炸事件。瓦斯已成为导致我国煤矿特大恶性事故的“头号杀手”。
(1)瓦斯存在于煤层及周围岩层中,是井下有害气体的总称。瓦斯属于________(选填“纯净物”或“混合物”)。
(2)当瓦斯爆炸时,下列自救措施不当的是___________。
A.站在原地不动
B.背对爆炸地点迅速卧倒
C.若眼前有水,应俯卧或侧卧于水中,并用湿毛巾捂住口鼻
D.选择合适通道迅速逃生
(3)煤矿瓦斯爆炸有三个必须条件:瓦斯纯度达到爆炸极限.足够的_______和________。对任何一个条件的有效控制都可避免瓦斯爆炸。这类事故的发生也提醒我们在做易爆.有毒气体的实验时应注意________________(任写一点)
21.下面4个观点都是错误的,写出你熟悉的化学反应方程式,否定相应的各错误观点:

22.(7分)某初级中学学生为了探究该校化学实验室的一种黑色粉末和一瓶标签破损的无色溶液(如图4所示)可能是什么物质,大胆猜想并设计实验进行验证。
![]()
[发现问题]当把黑色粉末与无色溶液混合时即产生气泡。
[查阅资料]初中化学实验室常见的黑色粉末有氧化铜.二氧化锰.四氧化三铁.
铁粉.炭粉等。
[提出假设]黑色粉末是 _____________,无色溶液是 __________ 。(只写一种假设)
[设计实验]向盛有少许黑色粉末的试管中加入适量的无色溶液;用_________ 收集一试管气体;
检验气体(写出操作方法)______________________ 。
[实验现象] ________________________________________________________________。
[实验结论]此气体是__________________,原假设 。
23.一定体积淡水中浮游植物在单位时间内经光合作用制造的有机物是该生态系统初级生产力。
6CO2+6H2O![]() C6H12O6+6O2
C6H12O6+6O2
生成有机物质量和O2的质量(设为m)的关系为____________________,所以由水体中溶解氧量的改变,可知生成有机物总量。
取水样,测定其中溶解氧量为m原。将水样灌满黑、白瓶后放到原先取水样的位置,经24h取出,测得黑.白瓶内水中溶解氧量为m黑、m白。黑瓶在无光条件下,水中浮游植物只发生消耗O2的呼吸作用,使水中溶解氧量下降;在光照条件下,白瓶内浮游植物发生光合作用使水中溶解氧量上升,同时植物也发生呼吸作用。已知黑.白瓶植物呼吸作用强度相同。下列二种溶解氧量的差值各表示什么?
m原--m黑:________________________________________________________
m白--m黑:________________________________________________________
三、实验题(本题包括3个小题,共20分)
24.(5分)向一定量的氯化钡溶液中加入一定量的硫酸钠溶液,充分反应后过滤。你认为滤液中溶质的组成最多有______种情况,这几种情况中一定都含有 。
请你设计一个实验,证明上述实验中氯化钡和硫酸钠刚好完全反应,并将有关内容填写在表中。

25.(7分)为探究CO2和NaOH确实发生了化学反应,某实验小组的同学设计出了下列4种实验装置,请回答下列问题:
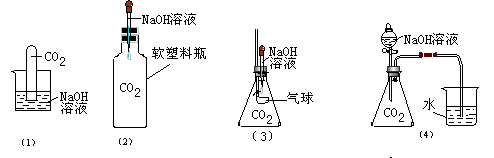
(1)选择任意一种实验装置,简述出现的实验现象,解释产生该实验现象的原因:选择的实验装置是__________,实验现象为:________________。产生该实验现象的原因是:________________________________________。
(2)某同学质疑上述实验设计,该同学质疑的依据是_______________。
(3)在原实验基础上,请你设计实验证明CO2和NaOH肯定发生了化学反应。
26.(8分)神舟五号.神舟六号载人航天飞船成功返航,标志着我国已跨入航天领域国际先进行列。
(1)在宇宙飞船上可以安装盛有Na2O2的装置,它的作用是与人呼出的二氧化碳反应生成氧气,写出该反应的化学方程式:______________________。
(2)请你写出一种实验室制取氧气的化学方程式:_________________。请在下面的仪器中根据上述反应选择适当的仪器组成一套制取并收集干燥的氧气的装置,各仪器从左到右的接口顺序是( )→( )→( )→( )。(填各仪器接口处的字母)。
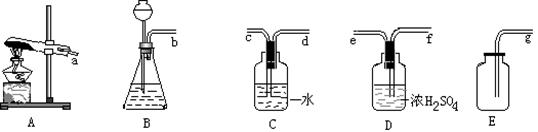
(3)证明集气瓶中的氧气已经收集满的方法是_____________________。
(4)要测定生成的氧气的体积,必须选用除上图以外的仪器是________(填仪器名称)。
四、计算题(本题包括2个小题,共9分)
27.(4分)已知CuO被C还原的产物是Cu2O(红色)。现有CuO和木炭粉组成的混合物4.24g,在高温下充分反应后,得到红色固体产物。反应后产生的气体能全部被过量的澄清的石灰水吸收,得沉淀2.00g。试计算所得红色固体产物质量。
28.(5分)学校研究性学习小组测定Cu--Fe合金.Fe--Zn合金和Fe--Al合金中铁的质量分数,实验室只提供一瓶未标明质量分数的稀硫酸和必要的仪器。
他们取其中一种合金的粉末5.6g与足量该硫酸充分反应,经测定,产生了气体a g。请讨论:当粉末为Fe--Al合金时,a>______;当粉末为Cu--Fe合金时,a<______;当_______> a >_______时,粉末可能是_________________。
(第十六届天原杯)复赛试题答案
一、选择题(本题包括15个小题,每小题2分,共30分。每小题有1个或2个选项符合题意。若有两个答案的错1个不得分,漏选1个扣1分。请将答案填在下表相应题号的空格内。)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 B D A C B C B C D B B B AC C AD
二、填空题(本题包括8个小题,共41分)
16、(3分)(1)6;6 (各1分,共2分)
(2)A2BC3等 (1分)
17、(5分)
(1)易溶于水,熔点271℃;(其它合理答案均可给分) (各1分,共2分)
(2)方法一:取少量待测物质与稀盐酸反应,若有红棕色气体产生,则该物质为亚硝酸钠。
或方法二:取待测物质加热到320℃以上,若有臭味气体产生,则该物质为亚硝酸钠。(3分)
18、(4分)
方法现象
(1)将两种化肥分别放入试管中加热 有刺激性气味气体产生,试管壁出现水珠,固体质量减少或消失的
(2)将两种化肥分别放入到装有稀盐酸的试管中 有无色无味的气体产生的
19、(7分)
(1) (每空0.5分,共3分)
A B C
酸 碱 盐
H2SO4或H2SO3或H2S NaOH Na2SO4或H2SO3或Na2S
(2)NaHSO4+NaOH→Na2SO4+H2O或2NaHSO4+Na2O→2Na2SO4+H2O
或2NaHSO4+Na2SO3→2Na2SO4+SO2↑+H2O或2NaHSO4+Na2S→2Na2SO4+H2S↑
(化学方程式答对1分得2分,共4分)
20、(5分) (每空1分,共5分)
(1)混合物 (2)A; (3)火源;氧气;点燃气体前要先检验气体的纯度(或应该在通风橱中进行实验或从遵守规章制度或注意安全等方面均可)
21、(6分) (每空1.5分)说明:其它合理答案均可给分。
(1)Cu(OH)2 CuO+H2O (2)CaCO3+2HCl→CaCl2+H2O+CO2↑
(3)2KMnO4 K2MnO4+MnO2+O2↑ (4)Ca(HCO3)2 CaCO3+H2O+CO2↑
22、(5分) (每空1分)
假设一:MnO2;H2O2;排水集气;用带火星的木条伸入试管中;带火星的木条复燃;O2;根据假设与检验的气体是否一致来判断成立或不成立。
假设二:铁粉;稀硫酸;排水(或向下排空气法);把收集满气体的试管移近酒精灯火焰(或把燃着的木条移近试管口);听到爆鸣声(或气体燃烧。火焰呈淡蓝色);H2;根据假设与检验的气体是否一致来判断成立或不成立。
23、(4分)(每空1分)有机物量=m×15/16 (180/192=15/16) (2分)
m原-m黑:24小时内浮游植物呼吸消耗氧量 (1分)
m白-m黑:24小时内植物籍光合作用制造有机物总量 (1分)
三、实验题(本题包括3个小题,共20分)
24、(5分)3;NaCl (每空1分,共2分)
验证的实验方法 可能观察到的实验现象 结论
(1)取样,加BaCl2溶液
(2)另取样,加Na2SO4溶液 无沉淀现象
无沉淀现象 滤液中无Na2SO4
滤液中无BaCl2
证明两者刚好完全反应
(每空1分,共3分)
25、(7分)(1) (1分)
装置(1) 装置(2) 装置(3) 装置(4)
实验现象 试管内液面上升,烧杯内液面下降(1分) 软塑料瓶变瘪(1分) 气球胀大(1分) 烧杯内的水流入锥形瓶中(1分)
产生 现象的原因 二氧化碳和氢氧化钠溶液反应,使试管内气体压强减少,液体被压入试管中(1分) 二氧化碳和氢氧化钠溶液反应,使塑料瓶内气体压强减少,大气压将软塑料瓶压瘪了(1分) 二氧化碳和氢氧化钠溶液反应,使锥形瓶内气体压强减少,大气使气球胀大(1分) 二氧化碳和氢氧化钠溶液反应,使锥形瓶内气体压强减少,大气压将液体压入锥形瓶(1分)
注:(1)~(4)只需答一题,本题共2分。
(2)二氧化碳溶解于水,使气体的量减少,也可以出现类似的现象。 (2分)
(3)往二氧化碳和氢氧化钠溶液作用后的液体中加入过量的稀盐酸,如果有无色无味的气体产生,说明二氧化碳和氢氧化钠溶液已经发生了化学反应。 (3分)
26、(8分)
(1)2Na2O2+2CO2→2Na2CO3+O2↑ (2分)
(2) 或2H2O2 2H2O +O2↑ (1分)
a,fe,g或b,fe,g (3分)
(3)带火星的木条放在g处,若复燃证明氧气已经收集满 (1分)
(4)量筒 (1分)
四、计算题(本题包括2个小题,共9分)
27、(4分)
解:4.24g混合物中,m(C): ×12=0.24g (1分)
M(CuO):4.24g-0.24g=4g (1分)
CuO全部被还原为Cu2O的化学方程式:
4CuO+C→2Cu2O +CO2
4×80 2×144
4.00 x
X=3.60(g) (2分)
28、(5分)
解:0.20;0.20;0.2~0.17; Fe-Zn合金或者Cu–Fe合金 (每空1分)
