初三级 班 姓名: 学号:
试卷说明:1.考试时间100分钟,试卷满分100分。
2.可能用到的相对原子质量:H—1,C—12,O—16,Na—23,Mg—24,S
—32,Cl—35.5,K—39,Ca—40,Fe—56,Cu
—64,Zn—65,Ba—137。
一、选择题(每小题只有1个选项符合题意,每小题1分,共10分)
1.首届东亚运动会上作升空表演的“北京2000”飞艇内,充有一种既安全、密度又小的气体,该气体是( )
A.甲烷 B.氢气 C.氨气 D.氦气
2.下列变化中,属于物理变化的是( )
A.电解水 B.干冰气化 C.铁生锈 D.白磷自燃
3.食油在锅里由于过热着了火,离开火炉后仍不熄灭,此时最好是( )
A.立即浇水 B.把油泼掉 C.用砂盖火 D.盖上锅盖
4.下列化学方程式中正确的是( )
A.Fe Zn(NO3)2=Fe(NO3)2 Zn B.Mg 2HNO3=Mg(NO3)2 H2↑
![]() C.Zn 2AgCl=ZnCl2 2Ag D.
C.Zn 2AgCl=ZnCl2 2Ag D.
5.将NaNO3和KCl两种饱和溶液混合后无晶体析出,在加热蒸发时,开始有晶体析出,此晶体是( )
A.NaCl B.KNO3 C.KCl D.NaNO3
6.农业科技人员和农民建议:在利用温室生产时,可向温室内通入适量的二氧化碳。这是因为( )
A.CO2可使害虫窒息死亡从而防治病虫害 B.施用CO2可促进植物的光合作用
C.CO2可产生温室效应从而提高室温 D.CO2能灭火,施用后可防止火灾
7.X元素的化合价为 m价,Y元素的化合价为-n价。由X元素和Y元素组成的化合物的1个分子中,其原子个数( )
A.一定是m个 B.一定是n个
C.一定是(m n)个 D.可能是(m n)个
8.若要除去CO2气体中混有的少量CO气体,采用的方法是( )
A.把混合气体点燃,使CO燃烧生成CO2
B. 把混合气体通过足量的NaOH溶液
C.把混合气体缓缓通过过量、灼热的CuO粉末
D. 把混合气体由一个容器倾倒到另一个容器中
9.将溶质的质量分数一定的烧碱溶液加水稀释。下图中能正确表示加水量(m克)与溶液pH值关系的是( )

10.在pH=1的无色透明溶液中,不能大量共存的离子组是( )
①Al3 ,Ag ,NO-3,Cl-;②Mg2 ,NH 4,NO-3,Cl-;③Na ,Ca2 ,SO2-4,CO2-3;④Zn2 ,Na ,NO-3.SO2-4.
A.①② B.②③ C.②④ D.①③
二、选择题(每小题有1~2个选项是正确的,每小题2分。填入错误答案不得分。有两个正确答案,只填一个正确答案得1分。共10分)
11.某学生取用m克氯酸钾加热使之完全分解制氧气,在实验中他错把高锰酸钾当成二氧化锰混入氯酸钾中,其实验结果和加热m克氯酸钾MnO2的混合物相比,下列推断中正确的是( )
A.反应速率相同 B.反应速率加快
C.生成氧气量多 D.生成氧气量不变
12.检验某可燃烧化合物是否含有氢、碳、氧3种元素,在该物质完全燃烧后还必须进行的实验是:①用带火星的木条检验;②用无水硫酸铜检验;③用澄清石灰水检验;④对反应物、生成物进行称量。以下选项中正确的是( )
A.①②③④ B.②③④ C.①②③ D.②③
13.a,b,c,d分别代表盐酸、氯化钡、硝酸银、碳酸钠4种物质的溶液中的某一种。现将它们两两混合,产生的现象如下表所示。
a,b,c,d两两混合产生的现象
反应物
a b
c d
a d
c a
d b
反应现象
白色沉淀
白色沉淀
沉淀
白色沉淀
无色气体
由上可知,a,b,c,d,依次是( )
A.AgNO3,HCl,BaCl2,Na2CO3 B.AgNO3,HCl,Na2CO3,BaCl2
C.HCl,BaCl2,AgNO3,Na2CO3 D.BaCl2,Na2Cl3,AgNO3,HCl
14.在一定条件下,同一反应进行的快慢与反应物的质量分数成正比。现用100克、溶质的质量分数为30%的硫酸溶液与过量镁粉反应,为了使反应不致太快而又不影响生成氢气的总量,可向所用的硫酸中加入适量的( )
A.NaOH溶液 B.水 C.K2SO4溶液 D.Na2CO3溶液
15.甲、乙两烧杯中分别盛有等体积、等溶质的质量分数的硫酸溶液。向甲烧杯中放入m克镁,向乙烧杯中投入m克锌,完全反应后发现有一烧杯中金属有剩余。则各烧杯中原来含硫酸的质量x之值是( )
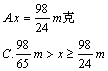
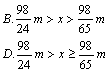
三、填空题(共25分,21题最后一空写出5个给1分,写3分或4个给1分,写出1分或2个不给分,其余每空1分)
16.在氢气、氧气、二氧化碳、氧化铜、碳、盐酸6种物质中(各空均用化学式表示):
(1)既有可燃性又有还原性的黑色固体是 ;
(2)少量存在于人的胃液中可帮助消化的是 ;
(3)工业上能用来制造氨气或盐酸的气体是 ;
(4)能使紫色石蕊试液变红的氧化物是 ;
17.由活性炭制成的冰箱除味剂是利用了活性炭的 作用。本炭使集气瓶中红标色的二氧化氮消失的变化是 变化。
18.把高梁、玉米等绿色植物的种子经过发酵、蒸馏,得到一种既可以用来制造饮料,又可做内燃机燃料的有机物,其名称为 ,化学式为 ,其燃烧的化学方程为
。
19.在氢气、氯酸钾、水、铜、氧化汞等物质中:
(1)属于金属单质的是 ;
(2)属于非金属单质的是 ;
(3)属于氧化物的是 ;
(4)属于化合物的是 ;
(5)化学式量最大的是 。
20.医药用的阿斯匹林的组成里含4.50%的氢、35.5%的氧、60.0%的碳,式量为180,阿斯匹林化学式为CxHyOz,则x= ,y= ,z= 。
21.某溶液中含有Na ,H ,Cl- ,SO2-44种离子,若滴入石蕊试液,则石蕊显 色;欲证实两种阴离子确实存在,应先加入适量的 溶液,使 完全转化为沉淀,过滤,再加入 溶液确定 的存在。原溶液中最多可有 种溶质,它们的化学式为 。
四、简答题(共23分)
22.为了提高我国的空气质量,可以采取的措施有哪此?
(1) ;
(2) ;
(3) ;
(4) 。
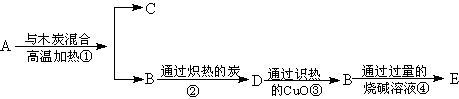 |
23.某黑色粉末A,溶于足量的稀硫酸中呈蓝色透明溶液。现将A进行如下图所示的处理:
(1)判定A,B,C,D,E各是什么物质?写出其化学式。
A ,B ,C ,D ,E 。
(2)写出各步反应的化学方程式:
① ;
② ;
③ ;
④ ;
24.家庭小实验:取一个玻璃杯,杯底放一支短蜡烛,并铺一层纯碱。把蜡烛点燃,沿杯壁倒入一些醋,观察到固体物质逐渐 ,同时有 产生。然后蜡烛 。
25.有X,Y,Z3种元素,它们的核内质子数均不超过18。它们相互之间能形成X2Z和YZ2型化合物。已知X 和Y原子的电子层数相同,Y原子比Z原子少2个电子,Z原子的最外层电子数是次外层电子数的3倍。这3种微粒结构示意图是X ,Y原子 ,Z元素的离子 。若将0.62克X2Z放入18.2克水中得A溶液,则溶液中溶质的质量分数为 ,pH值 7(填“>”,“<”,“=”)。
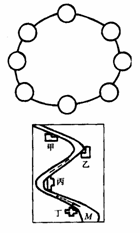
26.将①C,②CO2,③Fe,④CuO,⑤盐酸,⑥石灰水,⑦H2SO4,⑧Na2SO3溶液8种物质的序号分别填入下面右上图的圆圈内,使每个圆圈内的物质分别与其相邻的两种物质都能发生化学反应。
五、实验题(共20分)
27.在一条鱼、虾绝迹的小河边有4座工厂(箭头表示水流方向)甲、乙、丙、丁(见右下图)。每个厂所排出的废液里,分别含有Na2CO3、FeCl3 、Ca(OH)2、HCl中的一种。某中学环保小组对河水进行监测时发现:
①甲处河水呈乳白色;②乙处河水呈红褐色;③丙处河水由浑变清;④丁处产生气泡,河水仍清。请推断:
(1)4座工厂排出的废液里含有的污染物分别是:甲 ,乙 ,丙 ,
丁 。
(2)在M处取出的河水中肯定含有的离子是 。
28.下图是实验室中常用的装置。
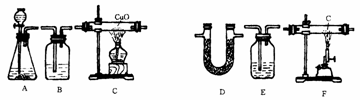
(1)若选用A,B,C,D组装仪器进行实验。片刻后D装置中硫酸铜由白变蓝,则A和C装置中发生的反应分别为(用化学方程式表示): 和 。在C装置中的粉末由 色变为 色。B装置中用于干燥气体的试剂是 .
(2)若按A,B,F,C,E顺序装配进行实验,A中的物质是石灰石和稀盐酸,E中的物质是澄清石灰水,则F和C中发生的反应的化学方程式分别为 和 。在E装置中观察到的现象是 ,反应的化学方程式为 。若E中的物质换成紫色石蕊试剂,则实验时观察到的现象为 ,如将溶液加热,则观察到的现象是
。
29.下图所示物质之间的转变,在一定条件下均可实现。
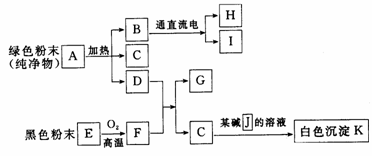
试分别写出下列所示物质的化学式。
A ,B ,C ,D ,F ,G ,J 。
六、计算题(共12分)
30.(4分)设t℃时NaOH的溶解度为110克,NaCl的溶解度为36.0克,在t℃时,取84.0克氢氧化钠饱和溶液与质量分数为29.2%的盐酸完全反应,求:
(1)需该质量分数的盐酸多少克?
(2)取上述反应后的溶液20克,其溶质的质量分数是多少?
31.(3分)今有氯酸钾和二氧化锰的混合物10克,其中二氧化锰2克,经加热一段时间后冷却,测得剩作固体中二氧化锰占25%,再把这些固体加热,问:还可以制得氧气多少克?
32.(5分)把一定量的硫酸铜和硫酸溶于水配成溶液。向盛 50克这种溶液的烧杯里加入8.5克铁粉,充分反应至蓝色完全消失和质量恒定(反应完全后铁粉有剩余),烧杯里的混合物的质量共为58.3克。过滤,并将滤出的不溶物洗涤,烘干,其质量为3.1克。计算:
(1)加入铁粉前的溶液中硫酸铜的质量分数是多少?
(2)反应后不溶物中铁与铜的质量比是多少?
(提示:根据质量守恒定律可知:生成氢气的质量应为反应前各组分的质量和减去反应后剩余的质量)
中考化学全真模拟试题(三)参考答案
一、1.D 2.B 3.D 4.D 5.A 6.B 7.D 8.C 9.D 10.D
二、11.B、C 12.B 13.A 14.B、C 15.D
三、16.(1)C (2)HCl (3)H2 (4)CO2
![]() 17.吸附,物理
17.吸附,物理
18.乙醇,C2H5OH,C2H5OH 3O2 2CO2 3H2O
19.(1)Cu (2)H2 (3)HgO和H2O (4)HgO、H2O、KClO3(5)HgO
20.9,8,4
21.红,Ba(NO3)2,SO2-4,AgNO3,Cl-,5,NaCl、Na2SO4、NaHSO4、HCl、H2SO4
四、22.(1)减少建筑工地粉尘
(2)限制使用含铅汽油
(3)尽量用燃气代替燃煤
(4)工业废气经处理后才能排放
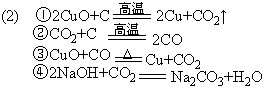 |
23.(1)A.CuO B.CO2 C.Cu D.CO E.Na2SO3
24.减少(或消失,或溶解),气泡,熄灭
25.
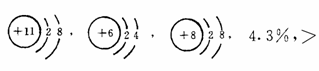
26.按顺时针方向填的顺序为①②⑥⑧⑦③⑤④(此题为2分)
五、27.(1)Ca(OH)2,FeCl3,HCl,Na2CO3(每空1分)
(3) ![]() Na 、Ca2 、Fe3 、H 、Cl-‑(此空2分)
Na 、Ca2 、Fe3 、H 、Cl-‑(此空2分)
![]()
![]() 28.(1)Z n H2SO4=ZnSO4 H2↑,H2 CuO Cu H2O,黑,紫红,浓H2SO4
28.(1)Z n H2SO4=ZnSO4 H2↑,H2 CuO Cu H2O,黑,紫红,浓H2SO4
(2)CO2 C 2CO,CO CuO Cu CO2, 溶液变浑浊,CO2 Ca(OH)2=CaCO3↓ H2O,溶液由紫变红,溶液由红变紫(每空1分)
29.A.Cu2(OH)2CO3 B.H2O C.CuO D.CO F.CuO G.Cu J.Ca(OH)2(每空0.5分)
六、30.(1)138克(2分)
(2)26.5%(2分)
31.1.1克(3分)
32.(1)8%(3分)
(2)15:16(2分)
