|
九年级期中化学测试卷
齐都中学 张燕 吕秋收
一、 选择题(每题2分,共50分)
1、 下列日常所见的溶液中呈酸性的是( )
A、肥皂水B、石灰水C、雪碧D、糖水
2、 使酚酞试液变红色的物质,能使紫色石蕊试液( )
A、变蓝色B、变无色C、变红色D、不变色
3、 向某溶液中滴入无色酚酞试液后不显色向该试液中滴入紫色石蕊试液则( )
A、一定显红色 B、可能为紫色,也可能为红色
C、可能显蓝色 D、一定显无色
4、 浓盐酸敞口放置一段时间后其溶质质量分数会( )
A、变大 B、变小 C、不变 D、无法确定
5、 下列方程式书写完全正确的是( )
A 、Zn 2HCl=ZnCl2 H2↑ B、2Fe 3H2SO4=Fe2(SO4)3 3H2 ↑
C 、Al HCl=AlCl3 H2↑ D、 Fe2O3 H2SO4=FeSO4 H2O
6、 下列物质属于碱的是( )
A、苛性钠 B、食盐 C、生石灰 D、石灰石
7、 下列说法中正确的是( )
A、酸碱一定含有氧元素,盐一定含有氧元素。
B、碱盐可能含有氧元素,酸一定含有氧元素。
C、盐一定含有金属元素,酸碱不一定含有金属元素。
D、酸碱一定含有氢元素,盐不一定含有金属元素。
8、 能用稀盐酸和金属直接反应制得的盐是( )
A、FeCl3 B、AlCl3 C、CuCl2 D、AgCl
9、 将下列物质溶于水后,所得溶液的PH最大的是( )
A、NaCl B、NaOH C、HNO3 D、CO2
10、 列物质长期放置在空气中,质量会增加且发生化学反应的是( )
A、浓盐酸 B、浓硫酸 C、生石灰 D、大理石
11、 鉴别氯化钠和硫酸钠两种溶液,可选用的最适宜的试剂是( )
A、BaCl2溶液 B、AgNO3溶液 C、MgSO4溶液 D、CuCl2溶液
12、 高锰酸钾俗称灰锰氧,其水溶液是常用的消毒剂。高锰酸钾的物质类别属于( )
A、酸 B、碱 C、盐 D、氧化物
13、下列溶液仍属于饱和溶液的是( )
A、饱和石灰水降温
B、饱和石灰水表面结了一层白膜
C、室温下的饱和硝酸钾溶液放进冰箱
D、向饱和蔗糖水里加水
14、钡餐透视检查时,若误服碳酸钡引起中毒,可立即服用下列那种试剂解毒( )
A、硫酸 B、硫酸镁 C、食盐水 D、食醋
15、生活中常见的下列物质不属于溶液的是()
A、糖水B、蒸馏水C、碘酒D、汽水
16、下列两种溶液混合后能发生化学反应,且溶液的总质量不会发生变化的是()
A、 氢氧化钾溶液和硫酸溶液 B、硝酸钠溶液和稀盐酸
C、食盐溶液和稀硝酸 D、三氯化铁溶液和烧碱溶液
17、从100克10﹪的氯化钠溶液中取出10克那么剩下的90克溶液的质量分数是()
A、1﹪B、90﹪C、10﹪D、11.1﹪
18、将氯化钾、氯化铁和硫酸钡的固体逐一分离,应选用的一组试剂是()
A、 水、硝酸银溶液、稀硝酸 B、水、氢氧化钠溶液、
C、水、氢氧化钾溶液、盐酸 D、水、氯化钾溶液
19、下列各组物质可按溶解、过滤、蒸发的操作顺序分离的是()
A、KCl和MnO2 B、KNO3和NaNO3
C、CuO和炭粉 D、水和植物油
20、下列制备氯化铜的方法正确的是()
A、 铜和稀盐酸反应 B、铜和稀硫酸反应后,再加稀盐酸
C、氢氧化铜和稀盐酸反应 D、氧化铜和稀硫酸反应
21、在一定温度下,将某物质的饱和溶液加水稀释成不饱和溶液,保持不变的是()
A、 溶剂的质量B、溶质的质量C、溶液的质量D、溶质的质量分数
22、用足量含有杂质(杂质不溶于水)的氯化钠配制100g溶质质量分数为10﹪的氯化钠溶液,实验操作有:①称量;②过滤;③蒸发结晶;④计算;⑤溶解;⑥洗涤干燥。其中操作顺序正确的是( )
A、⑤④②③⑥①⑤ B、④⑤②③①⑥⑤
C、⑤②③⑥④①⑤ D、④①⑤③⑥①⑤
23、分别取等质量的80℃的甲乙两种化合物的饱和溶液,降温至20℃后,所析出的甲的质量比乙的质量大(甲乙均不含结晶水)。下列关于甲乙溶解度的叙述中肯定正确的是( )
A、 温度对甲的溶解度影响较大
B、 温度对乙的溶解度影响较大
C、 80℃时,甲的溶解度比乙的大
D、20℃时,乙的溶解度比甲的大
24、在盛有硫酸铜饱和溶液的恒温密闭容器中,投入一块外形不规则的硫酸铜晶体,放置数天后,看到的现象是( )
A、 晶体部分溶解
B、 晶体外形和质量都不变
C、 晶体外形改变,质量不变
D、 晶体外形改变质量减小
25、欲除去氯化钙溶液中含有的少量盐酸,在不使用指示剂的情况下,应加入的试剂是( )
A、 石灰石粉末
B、 生石灰
C、 石灰水
D、 纯碱
二、 填空题(化学方程式和第5题每空2分,其余每空1分,共40分)
1.电镀前常用浓盐酸洗去镀件表面的铁锈,其化学方程式为:_________产生的现象是_________假如浸泡时间过长产生的现象______化学方程式_________
2.纯净的浓盐酸是___颜色的液体,常口放在空气中会出现___,这是因为____________放置一段时间后,液体的质量会___质量分数会___PH会___。用胃舒平(含氢氧化铝)治疗胃酸过多的化学反应原理化学方程式_________
3.海洋是巨大的资源宝库,从海洋中可以提取许多物质。请你参与下列物质的讨论:
⑴某盐场测得:①海水中含氯化钠约为3.5﹪ ;②在海边打深井,井水中含氯化钠约为8﹪ 。
晒盐最好选择___(填序号)作原料,理由是_________。
⑵晒盐原理说法正确的是___。
A、利用阳光和风力,使氯化钠蒸发出来
B、利用阳光和风力,是水分蒸发出来,析出盐
C、降低温度使氯化钠析出
D、日光照射后,氯化钠的溶解度变小
4、写出一种除去下列物质中的杂质的试剂的名称:(1)硝酸钾(氯化钾)
(2)氯化钠(硫酸钠) ,(3)铜粉(氧化铜)
5. 用一种物质鉴别下列物质:
⑴ KOH溶液、稀H2SO4、NaCl溶液,所用的试剂为___;
⑵ KOH溶液、石灰水、稀盐酸,所用的试剂为___;
⑶食盐、硝酸铵,烧碱所用的试剂___。
6. 物质A为常见的白色固体,A遇水后放出大量的热并生成微溶于水的白色粉末B;A,B与盐酸反应都生成C,C溶液与一种钠盐反应,生成难溶于水的D,D与盐酸又生成C则A___B___C___D___。
写出欧关反应的化学方程式:
 C D____________________________________________________ C D____________________________________________________
 D C_____________________________________________________ D C_____________________________________________________
7.如图是A、B、C三种固体物质的溶解度曲线。看图回答下列问题
⑴三种物质中,溶解度受温度影响最大的是____________ 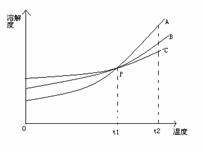
⑵P点的意义是____________
⑶t2。C时三种物质溶解能力由小到大的顺序是____________
⑷在t2。C时。用100g水配制A、B、C的饱和溶液,同时降到t1。C,析出晶体最多的是____________析出晶体最少的是____________
⑸除去A中混有少量的C,可以用____________方法
三、 计算题(10分)
100g硫酸铜溶液和100g氢氧化钠溶液恰好完全反应,得到的溶液的质量为190.2g ,求:氢氧化钠溶液中溶质的质量分数,所得溶液中溶质的质量分数。 (Cu : 64 S : 32 O : 16 Na : 23 H : 1)
参考答案
一.选择题
1.C 2.A 3.B 4.B 5.A 6.A 7.D 8.B 9.B 10.C 11.A 12.C 13.C 14.B 15.B 16.A 17.C 18.C 19.A 20.C 21.B 22.C 23.A 24.C 25.A
二.填空题
1.Fe2O3 6 HCl === 2FeCl3 3H2O ; 铁锈消失,溶液由无色变成黄色; 有气泡产生;
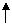 Fe 2HCl === FeCl2 H2 Fe 2HCl === FeCl2 H2
2.无;白雾;浓盐酸挥发出的氯化氢气体与空气中的水蒸气结合成盐酸笑液滴的缘故;减小;减小;增加; Al(OH)3 3 HCl == Al(OH)3 3 H2O
3.2; 氯化钠的含量高;B
4.硝酸银;氯化钡;盐酸
5.石蕊;碳酸钠;水
6.CaO; Ca(OH)2 CaCl2 CaCO3
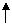 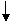 CaCl2 Na2CO3 ====CaCO3 2NaCl; CaCO3 2HCl=== CaCl2 H2O CO2 CaCl2 Na2CO3 ====CaCO3 2NaCl; CaCO3 2HCl=== CaCl2 H2O CO2
7.A; t10C时A.B.C三种物质的溶解度相同 ;C B A ;A ;C ;降温结晶
三.计算题
8% 7.47%
|