一、 选择题:
1、在炼铁、玻璃、水泥三种工业生产中,都需要用到的原料是( )。
( A )焦炭 ( B )石灰石 ( C )石英 ( D )纯碱
2、炼钢时加入氧化钙的主要作用是( )
( A )调整碳的含量 ( B )提高炉温
( C )把S、P、SiO2变为钢渣 ( D )降低钢的熔点
3、高炉炼铁时,加入焦炭的作用是( )
( A )作燃料提供热量 ( B )提供CO作还原剂
( C )作氧化剂 ( D )作催化剂
4、高炉炼铁时,加入石灰石的作用是( )
( A )氧化剂 ( B )除去脉石的造渣剂
( C )还原剂 ( D )除去硫、磷的造渣剂
5、炼钢时,在炼出的钢水中加入硅铁、锰铁等脱氧剂,目的是( )
( A )除去氧气 ( B )除去硫、磷等有害杂质
( C )除去过多的碳 ( D )除去过量的FeO和调节成分
6. 用来检验Fe3+是否存在的最佳试剂是( )
(A)H2S (B)NaOH (C)Na2CO3 (D)KSCN
7.w吨含杂质15%的赤铁矿石(主要成分是Fe2O3)可炼出含铁96%的生铁量的计 算式正确的是( )
( A )![]() ( B )
( B )![]() ÷(1-96%)
÷(1-96%)
( C )![]() ( D )
( D )![]() ×96%
×96%
二、 填空题:
8、FeS与盐酸反应,得到气体A和溶液B。取溶液2mL,通入适量的Cl2,得到溶液C,现象是____,其离子方程式是____,取溶液2mL,通入气体A,有____沉淀生成,其离子方程式是____,氧化剂是____,还原产物是____。
9、向含有FeCl3和BaCl2的溶液中,通入足量的SO2气体,有白色沉淀生成,过滤后,滤液中无Fe3+,写出有关的化学方程式________。
11、将等质量的锌、铁、铜3种金属的混合物A g加入氯化铁和盐酸混合溶液之中,充分反应后:
(1)若无固体剩余,则溶液中的阳离子一定有______,可能还有______。
(2)若剩余固体A/3g,则溶液中的阳离子一定有______,可能还有______,一定没有______。
(3)若剩余固体为3A/4g,则溶液中的阳离子一定有,一定没有______。
三、 计算题:
12、某高炉年生产铁400万吨(生铁中含碳为4%),问至少需要含Fe2O385%的赤铁矿多少万吨?
13、0.6mol/L的FeCl2溶液250mL,向其中通入一定量Cl2,反应后加水稀释至500mL,取出50 mL加足量AgNO3溶液得5.74g沉淀.求通入Cl2后稀释的溶液中Fe2+和Fe3+的物质的量浓度各多少?
答案
一、 选择题: 1、 B 2、 C 3、 AB 4、 B 5、 D 6、 A
二、 填空题:
7、溶液由浅绿色变为黄色,2Fe2++Cl2=2Fe3++2Cl-,2Fe3++H2S=2Fe2++S↓+2H+,Fe3+,Fe2+
8、2FeCl3+SO2+2H2O=2FeCl2+H2SO4+2HCl
BaCl2+H2SO4=BaSO4↓+2HCl
9、D
10、Fe2+、Zn2+、Cu2+,Fe3+、H+。
Zn2+、Fe2+,H+,Cu2+、Fe3+。
Zn2+,Cu2+、Fe3+。
三、 简答题:
四、 计算题:
11、Fe2O3 ~ 2Fe
![]()
x=645.4(万吨)
答:需铁矿石645.5万吨
12、Ag++Cl-===AgCl↓
500mL 稀释液中含Cl-物质的量为:
![]()
0.6mol/L,250mL FeCl2溶液中含FeCl2物质的量为:
![]()
2 FeCl2+Cl2=== 2FeCl3
通入Cl2的物质的量为:
![]()
∴通Cl2后FeCl2物质的量浓度为:
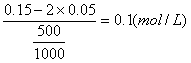
FeCl3溶液的物质的量浓度为: 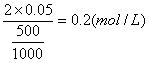
答: (略)
