|
РХГыЎЎЎЎЎЎЎЎЎЎ °ај¶ ЎЎЎЎЎЎЎЎ
Т»Ўў СЎФсМвЈә
ЎЎ 1ЎўФЪБ¶МъЎўІЈБ§ЎўЛ®ДаИэЦЦ№ӨТөЙъІъЦРЈ¬¶јРиТӘУГөҪөДФӯБПКЗ(ЎЎЎЎ )ЎЈ
ЎЎ ( A )Ҫ№МҝЎЎЎЎ ( B )КҜ»ТКҜЎЎЎЎЎЎ ( C )КҜУўЎЎЎЎ ( D )ҙҝјо
ЎЎ 2ЎўБ¶ёЦКұјУИлСх»ҜёЖөДЦчТӘЧчУГКЗ(ЎЎЎЎ )
ЎЎ ( A )өчХыМјөДә¬БҝЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎ( B )МбёЯВҜОВ
ЎЎ ( C )°СSЎўPЎўSiO2ұдОӘёЦФьЎЎЎЎЎЎЎЎ ( D )ҪөөНёЦөДИЫөг
ЎЎ 3ЎўёЯВҜБ¶МъКұЈ¬јУИлҪ№МҝөДЧчУГКЗ(ЎЎЎЎ )
ЎЎ ( A )ЧчИјБПМṩИИБҝЎЎЎЎЎЎ ( B )МṩCOЧч»№ФӯјБ
ЎЎ ( C )ЧчСх»ҜјБЎЎЎЎЎЎЎЎЎЎЎЎ ( D )ЧчҙЯ»ҜјБ
ЎЎ 4ЎўёЯВҜБ¶МъКұЈ¬јУИлКҜ»ТКҜөДЧчУГКЗ(ЎЎЎЎ )
ЎЎ ( A )Сх»ҜјБЎЎЎЎЎЎ ( B )іэИҘВцКҜөДФмФьјБ
ЎЎ ( C )»№ФӯјБЎЎЎЎЎЎ ( D )іэИҘБтЎўБЧөДФмФьјБ
ЎЎ 5ЎўБ¶ёЦКұЈ¬ФЪБ¶іцөДёЦЛ®ЦРјУИл№иМъЎўГММъөИНССхјБЈ¬ДҝөДКЗ(ЎЎЎЎ )
ЎЎ ( A )іэИҘСхЖшЎЎЎЎЎЎЎЎЎЎЎЎ ( B )іэИҘБтЎўБЧөИУРәҰФУЦК
( C )іэИҘ№э¶аөДМјЎЎЎЎЎЎЎЎ ( D )іэИҘ№эБҝөДFeOәНөчҪЪіЙ·Ц
ЎЎ 6. УГАҙјмСйFe3+КЗ·сҙжФЪөДЧојСКФјБКЗ(ЎЎ )
(A)H2SЎЎ (B)NaOHЎЎ (C)Na2CO3 ЎЎЎЎ(D)KSCN
ЎЎ 7.w¶Цә¬ФУЦК15%өДіаМъҝуКҜ(ЦчТӘіЙ·ЦКЗFe2O3)ҝЙБ¶іцә¬Мъ96%өДЙъМъБҝөДјЖЎЎ ЛгКҪХэИ·өДКЗ(ЎЎЎЎ )
ЎЎ ( A )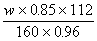 ЎЎЎЎЎЎЎЎ ( B ) ЎЎЎЎЎЎЎЎ ( B ) ЎВ(1Јӯ96%) ЎВ(1Јӯ96%)
ЎЎ ( C )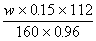 ЎЎЎЎЎЎЎЎ ( D ) ЎЎЎЎЎЎЎЎ ( D )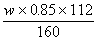 ЎБ96% ЎБ96%
¶юЎў МоҝХМвЈә
ЎЎ 8ЎўFeSУлСОЛб·ҙУҰЈ¬өГөҪЖшМеAәНИЬТәBЎЈИЎИЬТә2mLЈ¬НЁИлККБҝөДCl2Ј¬өГөҪИЬТәCЈ¬ПЦПуКЗ____Ј¬ЖдАлЧУ·ҪіМКҪКЗ____Ј¬ИЎИЬТә2mLЈ¬НЁИлЖшМеAЈ¬УР____іБөнЙъіЙЈ¬ЖдАлЧУ·ҪіМКҪКЗ____Ј¬Сх»ҜјБКЗ____Ј¬»№ФӯІъОпКЗ____ЎЈ
9ЎўПтә¬УРFeCl3әНBaCl2өДИЬТәЦРЈ¬НЁИлЧгБҝөДSO2ЖшМеЈ¬УР°ЧЙ«іБөнЙъіЙЈ¬№эВЛәуЈ¬ВЛТәЦРОЮFe3+Ј¬РҙіцУР№ШөД»ҜС§·ҪіМКҪ________ЎЈ
ЎЎ
11ЎўҪ«өИЦКБҝөДРҝЎўМъЎўНӯ3ЦЦҪрКфөД»мәПОпA gјУИлВИ»ҜМъәНСОЛб»мәПИЬТәЦ®ЦРЈ¬ід·Ц·ҙУҰәуЈә
ЈЁ1Ј©ИфОЮ№ММеКЈУаЈ¬ФтИЬТәЦРөДСфАлЧУТ»¶ЁУР______Ј¬ҝЙДЬ»№УР______ЎЈ
ЈЁ2Ј©ИфКЈУа№ММеA/3gЈ¬ФтИЬТәЦРөДСфАлЧУТ»¶ЁУР______Ј¬ҝЙДЬ»№УР______Ј¬Т»¶ЁГ»УР______ЎЈ
ЈЁ3Ј©ИфКЈУа№ММеОӘ3A/4gЈ¬ФтИЬТәЦРөДСфАлЧУТ»¶ЁУРЈ¬Т»¶ЁГ»УР______ЎЈ
ИэЎў јЖЛгМвЈә
12ЎўДіёЯВҜДкЙъІъМъ400Нт¶ЦЈЁЙъМъЦРә¬МјОӘ4ЈҘЈ©Ј¬ОКЦБЙЩРиТӘә¬Fe2O385%өДіаМъҝу¶аЙЩНт¶ЦЈҝ
13Ўў0.6mol/LөДFeCl2ИЬТә250mL,ПтЖдЦРНЁИлТ»¶ЁБҝCl2,·ҙУҰәујУЛ®ПЎКНЦБ500mL,ИЎіц50 mLјУЧгБҝAgNO3ИЬТәөГ5.74gіБөн.ЗуНЁИлCl2әуПЎКНөДИЬТәЦРFe2+әНFe3+өДОпЦКөДБҝЕЁ¶Иёч¶аЙЩ?
ҙр°ё
Т»Ўў СЎФсМвЈәЎЎЎЎ 1Ўў B ЎЎ2Ўў C ЎЎ3Ўў AB ЎЎ4Ўў B ЎЎ5Ўў D ЎЎ6Ўў A
¶юЎў МоҝХМвЈә
ЎЎ 7ЎўИЬТәУЙЗіВМЙ«ұдОӘ»ЖЙ«Ј¬2Fe2++Cl2=2Fe3++2Cl-Ј¬2Fe3++H2S=2Fe2+Ј«SЎэ+2H+Ј¬Fe3+Ј¬Fe2+
ЎЎ 8Ўў2FeCl3+SO2+2H2O=2FeCl2+H2SO4+2HCl
BaCl2+H2SO4=BaSO4Ўэ+2HCl
ЎЎ 9ЎўD
ЎЎ 10ЎўFe2Ј«ЎўZn2Ј«ЎўCu2Ј«Ј¬Fe3Ј«ЎўHЈ«ЎЈ
Zn2Ј«ЎўFe2Ј«Ј¬HЈ«Ј¬Cu2Ј«ЎўFe3Ј«ЎЈ
Zn2Ј«Ј¬Cu2Ј«ЎўFe3Ј«ЎЈ
ИэЎў јтҙрМвЈә
ЛДЎў јЖЛгМвЈә
ЎЎ 11ЎўFe2O3 ~ 2Fe
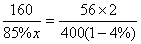
x=645.4(Нт¶Ц)
ҙрЈәРиМъҝуКҜ645.5Нт¶Ц
ЎЎ 12ЎўAg+Ј«ClЈӯ===AgClЎэ
500mL ПЎКНТәЦРә¬ClЈӯОпЦКөДБҝОӘЈә
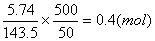
0.6mol/L,250mL FeCl2ИЬТәЦРә¬FeCl2ОпЦКөДБҝОӘЈә
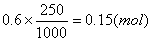
2 FeCl2Ј«Cl2=== 2FeCl3
НЁИлCl2өДОпЦКөДБҝОӘЈә
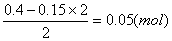
ЎаНЁCl2әуFeCl2ОпЦКөДБҝЕЁ¶ИОӘЈә
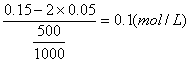
FeCl3ИЬТәөДОпЦКөДБҝЕЁ¶ИОӘЈә 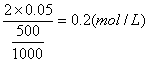
ҙрЈә (ВФ)
|