中考模拟测试试题(二)
化学试卷
可能用到的相对原子质量: H:1 C:l2 N:14 O:16 Na:23 S:32 Fe:56 Cu:64
第一部分 选择题 (共40分)
一、选择题(每道选择题有四个选项,其中只有一项符合题意。请用铅笔在答题卡上作答。选错、不选、多选或涂改不清的,均不给分)
1.下列自然现象中属于化学变化的是
A.海水蒸发 B.甲烷燃烧 C.山体滑坡 D.冰雪融化
2.组成空气中体积分数最高的气体单质的元素和人体中质量分数含量最高的元素分别
A.N、F B.O、C C.N、O D.O、H
3.蛋白质、糖类、油脂、维生素、无机盐、水六大类通称为营养素,是人类维持生命和健康必需物。下列常见物质中,含有较丰富蛋白质的是
eq \o\ac(○,1)1 白糖 eq \o\ac(○,2)2 花生油 eq \o\ac(○,3)3 鸡蛋 eq \o\ac(○,4)4 红萝卜 eq \o\ac(○,5)5猪瘦肉
A.③⑤ B. ①②③④ C.①③ D.②③⑤
 4.下列是一些常用的危险品图标,装运浓酸或浓碱的试剂罐外应张贴的图标是
4.下列是一些常用的危险品图标,装运浓酸或浓碱的试剂罐外应张贴的图标是



自燃物品 爆炸品 有毒品 腐蚀品
A B C D
5.下列物质都含有氧元素,从物质分类上看,它们都属于
①NaNO3 ②CuSO4 ③CaCO3 ④KMnO4
A.氧化物 B.金属氧化物 C.盐 D.酸
6.物质的用途主要由其化学性质决定的。下列用途与其化学性质关系正确的是
A
B
C
D
性质
石墨有导电性
活性炭有还原性
酸与金属氧化物反应
食盐能与硝酸银溶液反应
用途
铅笔芯
做除臭味吸附剂
用盐酸除铁锈
食物调味
7.下列说法不正确的是
A.油漆覆盖在钢铁制品的表面,能缓慢钢铁的生锈 B.陶瓷餐具是由有机合成材料制成
C.点燃办法鉴别涤纶和纯羊毛 D.肥皂水能区别硬水和软水
|
X |
|
2 |
|
8 |
|
Y |
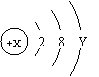 8.某粒子W的结构示意图如右图所示,下列对它的说法不正确的是
8.某粒子W的结构示意图如右图所示,下列对它的说法不正确的是
A.若X=16,Y=8,该粒子表示阴离子
B.若X=18,Y=8,该粒子表示原子
C.若X=l1,它的氧化物化学式为W2O
D.若X=15,原子核外电子数为15,它属于金属元素的原子
9.亚硝酸钠(NaNO2)的外观与食盐很相似,有咸味,误食易中毒。区别它们的一种方法是:将两者分别加热到320℃,没有明显现象的是食盐,能分解出一种具有刺激性气味气体的是亚硝酸钠,该气体可能是
A.CO2 B.SO2 C .NO2 D.HC l
1 0.玻璃棒在化学实验中有多种用途,下列实验操作中不需要用玻璃棒的是
A.用过氧化氢溶液制氧气 B.溶解食盐固体
C.过滤浑浊液 D.检验某溶液的pH值
11.“绿色化学”特点之一是充分利用能源,减少废物向环境排放。下列实验符合“绿色化
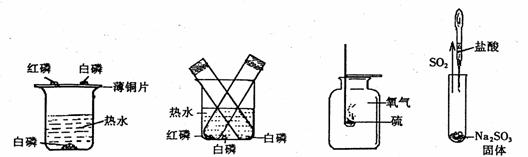 学“的是
学“的是
探究燃烧条件实验 探究燃烧条件实验 硫在氧气中 燃烧酸和盐反应
A B C D
12.进行化学实验必须注重安全,若发生事故要冷静处理。下列处理事故方法不正确的是
A.不慎将燃着的酒精灯碰倒产生火焰,应立即用湿布或砂盖灭
B.不慎电线短路引起电器着术,立即用二氧化碳灭火器扑灭
C.不慎将浓硫酸沾到皮肤上;应立即用大量水冲洗,再途上4%的碳酸氢钠溶液
D.不慎将白磷洒落在桌面上并自燃,应立即报告老师,若老师不在可打电话通知119
13.化学实验基本操作是否规范往往会影响实验的成败。下列实验基本操作正确的是
A.用10mL量筒和胶头滴管量取7mL食盐溶液
B.用胶头滴管吸取氢氧化钠溶液后,将滴管平放在桌面上,以免污染原溶液
C.给试管中的液体加热时,液体不得超过试管容积的 ![]()
D.把水小心地注入浓硫酸中,不断搅拌,得到稀硫酸
14.硝酸铵(NH4NO3)一种常见的氮肥,下列对它的说法正确的是
A.硝酸铵加碱有刺激性气味的氨气产生 B.硝酸铵中氮元素的化合价均为 5
C.硝酸铵中氮元素的质量分数为17.5% D.硝酸铵属于酸类
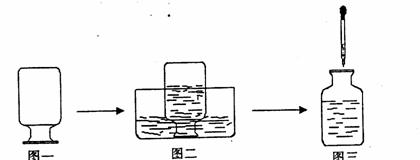 15.从某气体的实验过程(见下图),能够得出该气体的性质是
15.从某气体的实验过程(见下图),能够得出该气体的性质是
某气体放置方法 某气体放入水槽后情况 取出溶液后滴入酚酞试液,溶液变红色
①气体能与氧气 ②气体溶于水后溶液显碱性 ③气体有毒
④气体易溶手水 ⑤气体的密度比空气小
A.①②④⑤ B ①③ C ②⑤ D②④⑤
16.一些植物的花瓣可以制作成指示剂。以下是一些花汁在乙醇、酸、碱中的颜色表。试
分析,在玫瑰汁中加入PH大于7的溶液后呈现的颜色是
花的种类
花汁在乙醇中的颜色
花汁在酸中的颜色
花汁在碱中的颜色
大红花
粉红色
橙色
绿色
玫瑰
粉红色
粉红色
绿色
万寿菊
黄色
黄色
黄色
A.粉红色 B 绿色 C 黄色 D 橙色
17.下列除去杂质的方法能达到目的的是
物质
杂质
除杂方法
A
MnO2
NaCl
加水溶解、过滤、蒸发滤液、结晶
B
BaSO4
BaCO3
加足量稀盐酸、过滤、洗涤沉淀物、干燥固体
C
CuO
Cu
加足量稀盐酸、过滤、洗涤沉淀物、干燥固体
D
KCl
K2CO3
加足量稀硫酸、过滤、蒸发滤液、结晶
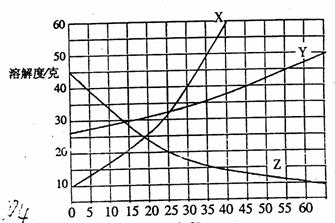 18.通过查阅右图物质的溶解度表;
18.通过查阅右图物质的溶解度表;
在30℃时,100g水中分别加入35g的X、Y、Z物质,得到的溶液是饱和的是
A.只有Z物质
B.X物质和Y物质
C.Y物质和Z物质
D.全部都是
19.向AgNO3、Cu(NO3)2、Zn(NO3)2混合溶液中,加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气体生成,则滤出的固体中
A.只有Fe B.可能有Ag、Cd C.一定有Zn和Fe D.一定有Ag、Cu、Fe
20.甲、乙、丙、丁是由Na、S、O、H四种元素中的两种或三稗元素组成的四种化合 物,能发生如下反应:
甲 BaCl2 → 两种盐; 乙 丙→盐 H2O; 丁 Na→NaOH
则下列推论中正确的是
A.甲一定是Na2SO4 B.乙一定是NaOH C.丙一定是H2SO4 D.可能是H2O
第二部分 非选择题 (共60分)
二、本题包括7小题,共34分
21.(2分)核糖是人类生命活动不可缺少的物质。已知核糖中含碳元素质量分数为40%,则120g核糖中含有碳元素质量为 。
22.(2分)用元素符号或化学式表示:
(1)n个氮气分子 (2)5个钠离子 。
23.(5分)加热高锰酸钾和加热氯酸钾都有 生成,写出加热氯酸钾发生反应的化学方程式 。将高锰酸钾与氯酸钾混合加热,其反应速率与只用氯酸钾加热的反应速率相比 (“快”或“慢”)。原因是
24.(8分)工业上为了测定硫酸的浓度(溶质的质量分数),常用一定标准浓度的氢氧化钠溶液与硫酸反应,化学反应方程式是 。
(1)首先,配制质量分数为10%的氢氧化钠溶液120g,需要 g氢氧化钠固体和水 g
(2)配制质量分数为10%的氢氧化钠溶液操作步骤见下图,正确的操作顺序是
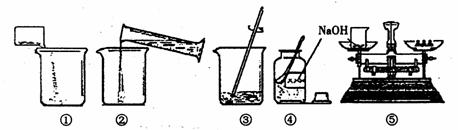
(3)用上述配好的10%氢氧化钠溶液40g与硫酸反应,以酚酞作指示剂,当看到混合溶液的颜色由红色刚好变为无色时,记录反应中耗用硫酸溶液质量为98g,则该硫酸的溶质质量分数是
25.(2分)用测定1m3被干燥的空气中尚剩余的水蒸汽含量(g)的多少来比较各种干燥剂的干燥效率。水蒸汽含量越少,干燥剂的干燥效率越高。下表列出常用干燥剂的干燥效率:
干燥剂
CuSO4
NaOH
KOH
浓H2SO4
水蒸汽含量(g/m3)
请问,干燥CO2最好选用 干燥剂,干燥O2最好选用 燥剂。
26.(6分)二氧化碳气体是我们在生活中常见的气体,请按题目的要求写出有二氧化碳参加或生成的化学反应方程式。
(1)由SO2等气体形成的酸雨(H2SO4)腐蚀天安门前的华表:
(2)用石灰水刷过的墙壁过一段时间变白变硬:
(3)甲烷燃烧产生热量:
|
硫酸 |
|
金属E ③ |
|
④ 碱Z |
|
黑色 固体丙 |
|
无色 溶液 |
|
黑色 固体丁 ② |
|
气体C ① |
|
金属F |
|
气体 A |
|
金属E |
|
黑色固体甲 |
|
黑色固体乙 |
|
金属E |
|
气体B |
|
金属F |
|
H2O |
|
溶液X |
|
溶液Y |
|
白色沉淀 |
|
蓝色沉淀 |
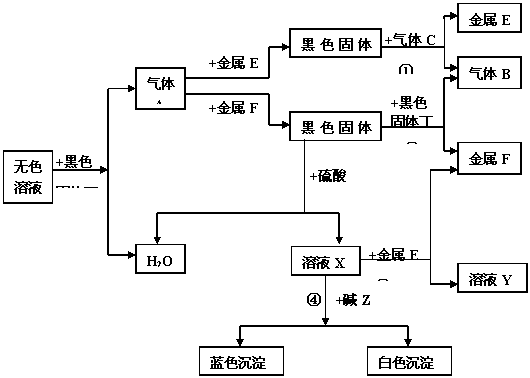 27.(9分)下图是常见物质间相互转化的关系图。已知金属F、E的相对原子质量之差为8,其他反应条件已省略。
27.(9分)下图是常见物质间相互转化的关系图。已知金属F、E的相对原子质量之差为8,其他反应条件已省略。
据上图关系回答:
(2)反应 eq \o\ac(○,2)2的基本反应类型是 反应
(3)写出反应 eq \o\ac(○,1)1 eq \o\ac(○,3)3 eq \o\ac(○,4)4的化学方程式:
eq \o\ac(○,1)1
eq \o\ac(○,3)3
eq \o\ac(○,4)4
三、本题包括4小题,共26分
28.(6分)实验室提供如下图所示的仪器:
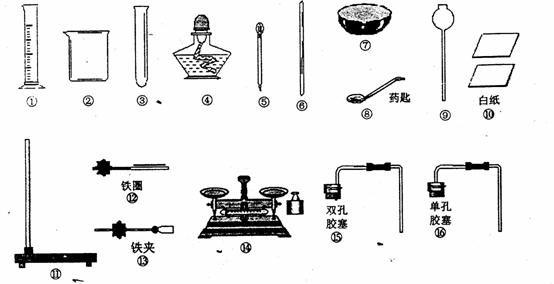
(1)指出下列仪器名称:
③ ; ④ ; ⑤
(2)完成下列化学实验,需要的仪器是(用编号回答):
eq \o\ac(○,1)1称量15g的食盐固体,需要的仪器是
eq \o\ac(○,2)2蒸发饱和食盐溶液的过程中,使用 仪器可防止溶液飞溅出来。
eq \o\ac(○,3)3实验室制二氧化碳,需要的仪器除 eq \o\ac(○,3)3 eq \o\ac(○,11)11 eq \o\ac(○,13)13 eq \o\ac(○,15)15用外,还需要的仪器是
29.(6分)按下图装置进行实验,玻璃管A中的黑色粉末可能是纯净物或混合物。
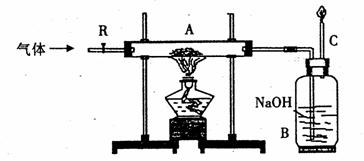
(1)打开活塞R,若通人CO2气体,C处有可燃性气体燃烧,则A处黑色粉末是
A处反应的化学方程式为 C处的作用是
(2)若关闭活塞R, 加热后A处黑色粉末变为红色, 则A处黑色粉末是 , B、C处没有明显现象。若要证实B中确实发生了化学反应,生成新的物质,实验方法和观察到的现象是 。
30.(8分)通过化学实验鉴别物质的存在,现象分析和推理过程是十分重要的。现有固体混合物一包,可能由KNO3、NaCl、K2SO4、BaSO4、CaCl2、Na2CO3中的一种或几种组成,依次进行实验,请完成如下实验记录分析报告。
实验步骤
观察现象
对应的推理和分析
eq \o\ac(○,1)1向混合物中加入适量水
全部溶解,溶液无色透明
eq \o\ac(○,1)1一定没有:
eq \o\ac(○,2)2向步骤 eq \o\ac(○,1)1溶液中滴加
过量BaC l2溶液
白色沉淀
eq \o\ac(○,2)2可能有:
eq \o\ac(○,3)3取步骤 eq \o\ac(○,2)2的白色沉淀,
加入稀盐酸
白色沉淀全部消失
eq \o\ac(○,3)3一定有:
eq \o\ac(○,4)4在步骤 eq \o\ac(○,2)2的浊液中滴加
过量AgNO3溶液和稀HNO3
白色沉淀
eq \o\ac(○,4)4一定有NaCl和CaCl2
问:(1) 步骤 eq \o\ac(○,4)4推理分析是否正确,假如不正确, 说明原因, 假如正确不用论述:
(2)固体混合物不一定含有
31.(6分)已知CuSO4溶液显蓝色,该溶液中含有较多的Cu2 和SO42-离子 。
(1)提出问题:溶液的颜色是由什么离子引起的。
现有试剂:K 2SO4溶液 、NaOH溶液、BaCl2溶液、锌粉,
现有仪器:试管、烧杯、铁架台(带铁圈)、漏斗、滤纸、玻璃棒
(2)假设:溶液的蓝色是由引起的Cu2 -,而不是由SO42引起的,
(3)验证:
操作步骤
现象和结论
答案及评分意见
一、 选择题 (每小题只有一项符合题意,每小题2分,共40分)
题号
1
2
3
4
5
6
7
8
9
10
答案
B
C
A
D
C
C
B
D
C
A
题号
11
12
13
14
15
16
17
18
19
20
答案
B
D
A
A
D
B
B
C
D
A
二、本题包括7小题,共34分
评分说明:化学方程式评分方法(满分为2分),化学式错不给分,配平错扣1分,条件或箭头错本小题共扣l分。
21、(2分)48
22、(各1分,共2分)
(1)nN2 (2)5Na
23、(共5分)
氧气或O2 (l分); 2KCl ![]() 2KCl 3O2 ↑ (2分)[条件写催化剂或MnO2给分];
2KCl 3O2 ↑ (2分)[条件写催化剂或MnO2给分];
快(1分); 高锰酸钾受热分解生成的二氧化锰对氯酸钾分解有催化作用 (分)。
24,(共8分)2NaOH H2SO4====Na2SO4 2H2O (2分)
(1)12(1分); 108 (1分)。
(2)④⑤①②③(1分,错或漏一个本题不给分)。
(3)5%(3分)。
25、(各1分,共2分)浓 H2SO4 ;KOH。
26、(各2分,共6分)
(1)CaCO3 H2SO4====CaSO4 CO2↑ H2O
(2)Ca(OH)2 CO2====CaCO3↓ H2O
(3)CH4 2O2 ![]() CO2 2H2O
CO2 2H2O
27、(共9分)
O2 (l分); MnO2(l分); 置换(1分):
Fw3O4 4CO ![]() 3Fe 4CO2(2分)(条件写"
3Fe 4CO2(2分)(条件写" ![]() "可给分);
"可给分);
CuSO4 Fe ==== FeSO4 Cu(2分);
CuSO4 Ba(OH)2====Cu(OH)2 ↓ BaSO4 ↓(2分)。
三、本题包括4小题,共26分
28、(各1分,共6分)
(1)试管; 酒精灯; 胶头滴管。
(2) eq \o\ac(○,14)14⑧ (不写⑧不扣分写②不扣分);
29、(共6分)
(1)炭粉(I分), CO2 C ![]() 2CO (2分),
2CO (2分),
使有毒气体转化为无毒气体,减少对环境污染(1分)。
(2)氧化铜和炭粉(1分),取少量反应后的B溶液,滴入稀盐酸(或硫酸等酸),有气泡产生(1分)
30、(共8分)
①BaSO4(1分) ②K2SO4(1分)、Na2CO3(1分) ③Na2CO3 (1分);
(1)不正确,因为在步骤②引入Cl-,不能确定有NaCl存在(l分),由于一定有Na2CO3就不能有CaCl2存在(1分)。
(2)KNO3(1分)、NaCl(1分)。
31、(共6分)说明:本题答案有多种,能验证溶液的蓝色是由Cu2 引起的得3分,能验证溶液的蓝色不是由SO42-引起的得3分。答案只要合理则给分。
答案一:
操作步骤
现象和结论
用试管取少量的CuSO4溶液,加入过量的NaOH溶液(1分),过滤(1分)
用试管取少量的CuSO4溶液,加入过量的BaCl2,溶液(1分),过滤(1分)
产生蓝色沉淀,滤液为无色(1分),则溶液的蓝色是由Cu2 引起的。
产生白色沉淀,滤液仍为蓝色(1分)则溶液的蓝色不是由SO42-引起的。
答案一:
操作步骤
现象和结论
用试管取少量的CuSO4溶液,加过量的锌粉(1分)振荡,静置(1分)(或过
滤)。
观察地K2SO4溶液。(2分)
上层清液为无色(1分)(或滤液为无色)说明溶液的篮色是由Cu2 引起的。
K2SO4溶液是无色的(1分)说明溶液的蓝色不是由SO42-引起的。
© 2004-2010 中国哲士网版权所有 引用本站内容请指明来源 给本站投稿 备案序号 蜀ICP备05009253号
